Rümeysa
Forum Üyesi
- Katılım
- 22 Eyl 2022
- Mesajlar
- 1,349
- Puanları
- 0

Periyodik Tablo ve Grup İsimleri
Kimyasal elementlerin sınıflandırılması için oluşturulan periyodik tablo sıralaması elementlerin artan atom numaralarına göre yapılır. Her kimyasal elementin atom numarası farklıdır. Toplamda 118 adet element vardır. Söz konusu elementlerden 94 tanesi dünya üzerinde bulunmaktadır.
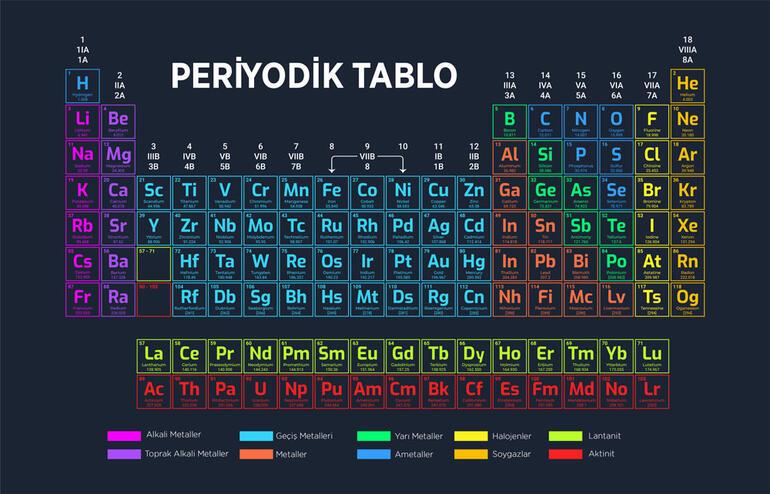
Periyodik tabloda dikey sütunlara grup denir. Aynı grupta olan elementlerin kimyasal özellikleri benzerdir. Aşağı doğru dikeyce indikçe özellik yoğunlaşır ve belirginleşir. Bir A grubuna ait elementin son katmanında kaç elektron varsa grup sıralaması da odur. Örneğin, berilyum (Be) atomunun son katmanında 2 elektron vardır ve bu atom 2A grubunun elementi olur.
Bir gruptaki elementlerde yukarıdan aşağıya doğru inildiğinde Atom yarıçapı artar, iyonlaşma enerjisi ve elektronegatiflik ise azalır.
Periyodik tabloda 8 tane A 8 tane de B grubu vardır. A grubu elementlerine baş grup elementleri de denir. Bazı grupların özel adları şöyledir.
- 1A grubu Alkali metal'ler denir. Hidrojen hariç hepsi metaldir.
- 2A grubu Toprak alkali metalleri denir. Hepsi metaldir.
- 3A grubu Toprak metalleri (ya da Bor grubu) olarak adlandırılır.
- 4A Karbon grubu olarak adlandırılır.
- 5A Azot grubu (ya da nitrojen grubu) olarak adlandırılır.
- 6A Oksijen (ya da Kalkojen) grubu olarak adlandırılır.
- 7A grubu Halojenler olarak adlandırılır.
- 8A grubu Soygazlar bu grupta yer alır.
1B'den başlamaz. 3B ile başlar. (2A dan sonra geldiğinden) 2B ile biter. (2B den sonra 3A gelir).
8B grubu yan yana 3'lü element gruplarından oluşur. 8B grubunda dikey benzerlikler yatay benzerliklerden daha önemlidir.
Periyodik Cetveldeki Elementlerin Özellikleri Nelerdir?
1. Hidrojen (H)

Hidrojen, periyodik tablonun 1. periyodunun 1. grubunda yer alan bir elementtir. Hidrojenin atom numarası 1'dir. Hidrojen, H sembolü ile gösterilir ve ametaldir.
Standart sıcaklık ve basınç altında renksiz, kokusuz, metalik olmayan, tatsız, oldukça yanıcı ve H2 olarak bulunan bir diatomik gazdır. 1,00794 g/mol'lük atomik kütlesi ile tüm elementler arasında en hafif olanıdır. Hidrojenin adı, Yunancada "su oluşturan" anlamına gelen idrogono kelimesinden gelir.
Hidrojen, evrenin kütlesinin %75'ini oluşturan ve evrende en çok bulunan elementtir. Ana hatta bulunan yıldızların çoğunluğu, plazma hâlinde olan hidrojenden oluşur. Elementel hidrojen Dünya'da az bulunur. Endüstride metan gibi hidrokarbonlardan üretilebildiği gibi, pahalı olsa da suyun elektrolizinden de üretilebilir.
2. Helyum (He)

Helyum, periyodik tablonun 1. periyodunun 18. grubunda yer alan bir elementtir. Helyumun atom numarası 2'dir. Helyum, He sembolü ile gösterilir ve soy gazdır.
Evrende hidrojenden sonra en yaygın bulunan ikinci elementtir.
Büyük Hadron Çarpıştırıcı'daki, uydu araçlarındaki, manyetik rezonans görüntüleme (MRI) sistemlerindeki süperiletken mıknatısları soğutmak için kullanılır.
Çok çabuk genleştiği için taşıtlardaki hava yastıklarını şişirmek için kullanılır.
Dalgıçlar ve basınç altında çalışanlar için üretilen yapay atmosfer %80 helyum, %20 oksijen karışımından oluşur.
Mağaza ve marketlerde kullanılan barkod okuyucularda helyum-neon gaz lazerleri kullanılır.
3. Lityum (Li)

Lityum, periyodik tablonun 2. periyodunun 1. grubunda yer alan bir elementtir. Lityumun atom numarası 3'tür. Lityum, Li sembolü ile gösterilir ve metaldir.
Doğada saf metal hâlde bulunmaz, bileşikler içinde bulunur. En önemli kullanım alanı cep telefonları, dizüstü bilgisayarlar, dijital fotoğraf makineleri vb. elektrikli cihazların şarj edilebilir pilleridir. Alüminyum ve magnezyumun sertliğini artırmak ve ağırlıklarını düşürmek için lityumlu alaşımları üretilir. Bu alaşımlar hava taşıtlarında ve yüksek hızlı trenlerde kullanılır. Psikiyatrik ilaçlarda az miktarda lityum karbonat kullanılır ancak fazlası zehirlidir.
4. Berilyum (Be)

Berilyum, periyodik tablonun 2. periyodunun 2. grubunda yer alan bir elementtir. Berilyumun atom numarası 4'tür. Berilyum, Be sembolü ile gösterilir ve metaldir.
Adını bulunduğu değerli taş olan berilden alır. Yer kabuğunda farklı minerallerde bulunur. Zümrüt ve akuamarin berilyum içeren değerli taşlardır.
Berilyum ve bileşikleri zehirli ve kanserojendir. Berilyum tozunun dumanının solunması akciğerlerde berillioz denilen kalıcı hasara yol açar.
Hava taşıtları, uzay araçları, füzeler ve iletişim uydularında berilyum alaşımları kullanılır.
Nükleer reaktörlerde yansıtıcı ya da nötron düzenleyici olarak kullanılır.
5. Bor (B)

Bor, periyodik tablonun 2. periyodunun 13. grubunda yer alan bir elementtir. Borun atom numarası 5'tir. Bor, B sembolü ile gösterilir ve yarı metaldir.
Yer kabuğunda farklı minerallerde bulunur. Dünya üzerindeki bor rezervlerinin %73'ü Türkiye'de bulunur. Tinkal, kolemanit, kernit ve boraks bor içeren minerallerdir.
Zehirli olarak değerlendirilmese de yüksek dozda alımı metabolizmayı olumsuz etkileyebilir. Ortalama bir insan, günlük yiyeceklerinden 2 mg bor alabilir.
Bitki hücrelerinin duvarlarının önemli bir bileşenidir.
Borlu bileşikler göz damlaları, antiseptik çözeltiler ve çamaşır deterjanlarında kullanılır. Ayrıca cam ve fayansların da dayanıklılığını artırırlar.
Bor-10 izotopu nötronları soğurabildiğinden nükleer reaktörlerde ve nötron algılayıcı cihazlarda kullanılır.
6. Karbon (C)

Karbon, periyodik tablonun 2. periyodunun 14. grubunda yer alan bir elementtir. Karbonun atom numarası 6'dır. Karbon, C sembolü ile gösterilir ve ametaldir.
*Karbon 3825ºC'de süblimleşir yani katı hâlden doğrudan gaz hale geçer.
**Elmas için 3513 g/cm3, grafit için 2,2 g/cm3'tür.
Elmas doğadaki en sert doğal malzeme olması ile bilinir ancak yeterince ısıtıldığında yanarak karbondiokside dönüşür ve gözden kaybolur. Elmasın saf karbon olduğu 1796'da bir yanma tepkimesiyle doğrulandı.
Saf karbon doğada çeşitli biçimlerde bulunur. Elmas, karbon atomlarının üç boyutta kristal yapı içinde düzenlenmesiyle oluşur. Hayli yumuşak bir malzeme olan grafitte ise karbon atomları iki boyutlu katmanlar içinde düzenlenir ve farklı katmanlar arasındaki bağlar zayıftır.
Endüstriyel elmaslar kayaçları kesmek ve delmek için matkap gibi aletlerde kullanılır.
Grafit, kurşun kalemlerde; aktif kömür (siyah renkte bir tür hafif karbon), filtreleme ve saflaştırmada kullanılır.
Fosil yakıtlarda bulunan hidrokarbonlar (karbon ve hidrojenden oluşan bileşikler) genellikle yakıt olarak kullanılsa da petrokimya endüstrisinde plastik, boya, polimer vb. üretiminde de kullanılır.
Çok dayanıklı ve hafif bir malzeme olan karbon fiber, kayak malzemesi ve olta gibi spor malzemelerinin yanı sıra roket ve hava taşıtlarında, yanmaz tekstil malzemeleri üretiminde kullanılır.
İki boyutlu malzemelerin bir örneği olan grafende, karbon atomları tek bir katman içinde düzenlenir. Grafen kullanılarak üretilen karbon nanotüpler ve atom ölçeğinde inceliğe sahip yüzeylerden, elektronik endüstrisindeki ve nanoteknolojideki araştırmalarda yararlanılıyor.
Bir sera gazı olan karbondioksit yeryüzünün yaşama elverişli bir sıcaklığa sahip olmasına katkıda bulunuyor. Ancak çağımızın en önemli çevre sorunlarından biri olan küresel iklim değişikliğinin ana sebeplerinden biri de insan etkinlikleri nedeniyle atmosferdeki karbondioksit oranının artmasıdır.
7. Azot (N)

Azot, periyodik tablonun 2. periyodunun 15. grubunda yer alan bir elementtir. Azotun atom numarası 7'dir. Azot, N sembolü ile gösterilir ve ametaldir.
Atmosferdeki havanın %78'i azottur. Azotun canlılar tarafından doğal yollarla taşınıp dönüştürülmesine "azot döngüsü" denir.
Kimya endüstrisinde gübre, naylon, boya ve patlayıcı yapımında kullanılır.
Azot gazı tepkimelere girmeye karşı isteksiz olduğu için yiyeceklerin uzun süre saklanmasında, diot ve transistör gibi elektroniklerin üretiminde kullanılır.
Sıvı azot ile temas ettiğinde canlı hücreler saniyeler içinde dondurulabilir.
8. Oksijen (O)

Oksijen, periyodik tablonun 2. periyodunun 16. grubunda yer alan bir elementtir. Oksijenin atom numarası 8'dir. Oksijen, O sembolü ile gösterilir ve ametaldir.
Suda kolayca çözünebilmesi oksijen solunumu yapan canlıların suda yaşamasını mümkün kılar.
Atmosferin %21'i oksijendir. Bu oran solunumun zorlaştığı %17'lik ve çoğu organik bileşiğin tutuştuğu %25'lik oranların tam ortalamasıdır.
Endüstrideki en yaygın kullanım alanı çelik üretimidir.
Metalleri kesmeye yarayan oksijen tabancalarında oksijen gazı kullanılır.
9. Flor (F)

Flor, periyodik tablonun 2. periyodunun 17. grubunda yer alan bir elementtir. Florun atom numarası 9'dur. Flor, F sembolü ile gösterilir ve ametaldir.
İkinci Dünya Savaşı'na kadar endüstriyel amaçlarla büyük miktarda flor üretimi yapılmıyordu. İkinci Dünya Savaşı sırasındaki atom bombası geliştirme çabaları ve diğer nükleer enerji projeleri yüksek miktarda flor üretimini gerekli kıldı. Bu tarihten önce buzlu cam üretiminde ve kaynak yapımında flor tuzları kullanılıyordu. Günümüzde nükleer enerji santrallerine uranyum yakıtı hazırlayan tesislerde uranyum izotoplarını ayrıştırmak için uranyum florür (UF6) bileşiği kullanılır.
Isıya dayanıklı plastiklerde, teflon kaplamalarda, kablo izolasyonu ve izolasyon bantları ile su geçirmez ayakkabı ve giysilerdeki Gore-Tex ürünlerde kullanılır.
Diş çürüklerini önlediği düşünüldüğü için içme sularına 2 mg/l'den az olmak üzere flor tuzları (metal-flor bileşikleri) katılır. Diş macunlarında da florür bulunur. Fazla miktardaki florür zehirlidir. Saf flor ise çok zehirlidir. Hidorflorik asit (HF), camı çözen tek asittir.
10. Neon (N)

Neon, periyodik tablonun 2. periyodunun 18. grubunda yer alan bir elementtir. Neonun atom numarası 10'dur. Neon, Ne sembolü ile gösterilir ve soy gazdır.
Doğada atmosferde ve kayaçların içinde hapsolmuş şekilde bulunur. Kararlı bir bileşiği yoktur.
Kütle numaraları 21, 22 ve 23 olan üç doğal izotopu bulunur. Neon birden fazla izotopunun kararlı olduğu anlaşılan ilk elementtir.
Zehirli değildir.
En yaygın kullanımı reklam panolarındaki "neon ışıkları" şeklindedir. Vakumlanmış bir tüpe doldurulan neon kırmızımsı turuncu renkte ışık yayar. Yalnızca kırmızı renkli pano ışıklarında saf neon bulunur.
Yıldırımsavarlarda, dalış ekipmanlarında ve lazerlerde kullanılır.
Sıvı neon önemli soğutuculardandır. Sıvı hidrojenden üç kat, sıvı helyumdan ise kırk kat fazla soğutma kapasitesi vardır.
11. Sodyum (Na)

Sodyum, periyodik tablonun 3. periyodunun 1. grubunda yer alan bir elementtir. Sodyumun atom numarası 11'dir. Sodyum, Na sembolü ile gösterilir ve metaldir.
Sodyum metali bazı nükleer reaktörlerde soğutucu olarak kullanılsa da sodyum tuzlarının kullanım alanı saf metalden daha fazladır.
Vücudumuzda sinir hücrelerinde sinyallerin iletilmesinin yanı sıra kan ve dokulardaki su seviyesinin düzenlenmesi gibi pek çok metabolik süreçte rol alır.
En yaygın sodyumlu bileşik, sofra tuzu olarak bilinen sodyum klorürdür. Ayrıca sodyum karbonat tuzu da yaygındır. Çamaşır sodası ya da su yumuşatıcı olarak kullanılır. Sodyum klorür ve sodyum karbonat tarih öncesi çağlardan beri bilinip kullanılsa da saf sodyumun elde edilmesi ancak 1807 yılında elektrik akımının kullanılmasıyla mümkün oldu.
12. Magnezyum (Mg)

Magnezyum, periyodik tablonun 3. periyodunun 2. grubunda yer alan bir elementtir. Magnezyumun atom numarası 12'dir. Magnezyum, Mg sembolü ile gösterilir ve metaldir.
Magnezyumun yoğunluğu alüminyumdan az olduğu için alüminyumla birlikte kullanıldığında ağırlığını fazla artırmadan sağlamlaştırır. Bu alaşımlar hava taşıtları ve araba üretiminde kullanılır.
Magnezyum çok çabuk tutuşup kıvılcımlar çıkararak yandığı için havai fişek ve yıldızsaçan gibi kıvılcım çıkaran ürünlerde kullanılır.
Bununla birlikte tuğlaları ve çeşitli boyaları ateşe dayanıklı hâle getirmek için kullanılır.
İçinde magnezyum bulunan lüle taşı (magnezyum silikat) çeşitli süs eşyalarının yapımında kullanılır.
Vücudumuzda yüzlerce enzimin çalışmasında rol alır ve kemikleri sağlamlaştırır.
Fotosentezi gerçekleştiren klorofil molekülünde magnezyum bulunur. Magnezyum olmasa fotosentez gerçekleşemez ve bildiğimiz anlamıyla bugün Dünya'daki biyolojik yaşam var olamazdı.
13. Alüminyum (Al)

Alüminyum, periyodik tablonun 3. periyodunun 13. grubunda yer alan bir elementtir. Alüminyumun atom numarası 13'tür. Alüminyum, Al sembolü ile gösterilir ve metaldir.
Yer kabuğunda en yaygın bulunan metaldir. Doğada çoğunlukla bileşikleri şeklinde bulunur.
Alüminyum yoğunluğu az, ısıyı iyi ileten, paslanmaya dayanıklı ve şekillendirmesi kolay olan bir elementtir.
Zehirli değildir.
Yiyeceklerle aldığımız alüminyumun çok azı emilir. Ortalamadan fazla alüminyum içeren yiyecekler şunlardır: çay, işlenmiş peynir ve mercimek. İçinde asitlik düzeyi yüksek yiyecekler pişirilmediği müddetçe alüminyum kaplarda pişirilen yemekler aldığımız alüminyum miktarını etkilemez.
Saf alüminyum yeterince dayanıklı değildir. Ancak alüminyum içeren alaşımlar mutfak gereçlerinden hava taşıtlarına, içecek kutularından alüminyum folyolara pek çok sektörde kullanılır.
14. Silisyum (Si)

Silisyum, periyodik tablonun 3. periyodunun 14. grubunda yer alan bir elementtir. Silisyumun atom numarası 14'tür. Silisyum, Si sembolü ile gösterilir ve yarı metaldir.
Silisyum yer kabuğunda en yaygın bulunan ikinci elementtir.
Silisyum bir yarı metaldir. Bilgisayar ve elektronik cihazların üretiminde yüksek saflıkta silisyum kullanılır. Silisyumun elektriksel özelliklerini kontrol etmek amacıyla içine az miktarda bor, galyum, fosfor ya da arsenik katılır.
Silikon (bir tür polimer) üretiminde kullanılır.
Silikon kauçuk banyolarda, pencere kenarlarında, boru sistemlerinde ve çatılarda su geçirmez yalıtım malzemesi olarak kullanılır.
Granit ve bazı diğer kayaçlar karmaşık silikatlardır ve inşaat sektöründe yoğun olarak kullanılırlar. Silisyum elementi barındıran kum ve kil ile beton ve çimento hazırlanır. Kum ayrıca camın da ana ham maddesidir.
Silisyum, silikat hâli ile çömlekçilikte, emaye mutfak gereçlerinde ve ısıya dayanıklı seramiklerde kullanılır.
Silisyum zehirli olmamasına rağmen belirli silikatların, örneğin asbestin, kanserojen etkisi vardır. Silisyumlu tozlara maruz kalan maden ve taş işçilerinde silikoz denilen tehlikeli bir akciğer hastalığı görülebilir.
Taş Devri'nde kullanılan ilk aletlerden olan çakmak taşları silisyumun oksitlenmiş hâli olan silika bazlı kayaçlardandır.
15. Fosfor (P)

Fosfor, periyodik tablonun 3. periyodunun 15. grubunda yer alan bir elementtir. Fosforun atom numarası 15'tir. Fosfor, P sembolü ile gösterilir ve ametaldir.
Doğada çoğunlukla kırmızı ve beyaz fosfor olmak üzere iki şekilde bulunur. Beyaz fosfor zehirlidir ve ciltle teması ciddi yanıklara sebep olabilir. Karanlıkta parlar ve havayla temas ettiğinde kendiliğinden tutuşabilir. Kırmızı fosfor ise zehirli değildir.
Beyaz fosfor ışık yayan ve yakıcı aletlerde kullanılır.
Kibritlerin tutuşturmak amacıyla kullanılması için kibrit kutularının kenarlarında bulunan malzemenin içinde kırmızı fosfor da vardır.
Fosforun en yaygın kullanım alanı gübre sanayiidir. Ayrıca belirli özelliklere sahip cam ve porselen yapımında da kullanılır.
Canlılarda DNA ve RNA'nın yapısında bulunur. Ayrıca canlılarda enerji transferinin gerçekleşmesini sağlayan ATP (adenozin trifosfat) molekülünün temel bileşenidir
16. Kükürt (S)

Kükürt, periyodik tablonun 3. periyodunun 16. grubunda yer alan bir elementtir. Kükürtün atom numarası 16'dır. Kükürt, S sembolü ile gösterilir ve ametaldir.
Sarı renkte, kristal şeklindedir ve çürük yumurta gibi kokar.
Kükürt tüm canlılar için hayati önem taşır. Amino asitlerden protein üretilmesi için gereklidir.
Kükürt zehirli değildir ancak karbon disülfür, hidrojen sülfür ve sülfür dioksit zehirlidir. Özellikle hidrojen sülfür solunum felcine sebep olarak ölüme yol açabilir.
Kömürle rafine edilmemiş yağın yakılması ile sülfür oksit açığa çıkar. Atmosferdeki sülfür dioksit asit yağmurlarına neden olabilir. Rafine edilmemiş fosil yakıtların yakılması ile sülfür dioksit atmosfere karışabilir.
Kauçuğun sertleştirilmesinde, siyah barut üretiminde ve mantar önleyici olarak kullanılır.
Kükürtün en önemli kullanım alanı sülfürik asit üretimidir. Sülfürik asitten de en çok gübrelerdeki fosfatı elde etmek için kullanılan fosforik asidin üretiminde yararlanılır.
Merkaptan denilen kükürtlü bileşikler doğal gaza eklenir. Keskin kokuları sebebiyle gaz kaçaklarının algılanmasını sağlarlar. Ayrıca haşere ve zararlı bitkileri öldürmek için üretilen kimyasal ilaçlarda ve gümüş parlatıcılarda da merkaptanlar kullanılır.
Kükürtlü bileşikler kâğıtları beyazlatmada kullanılır. Bu bileşikler gıda koruyucu, yüzey temizleyici ve deterjanlarda da kullanılır.
Çimento ve alçı üretiminde kullanılmak üzere her yıl yüz milyon ton civarında kalsiyum sülfat minerali çıkarılır.
17. Klor (Cl)

Klor, periyodik tablonun 3. periyodunun 17. grubunda yer alan bir elementtir. Klorun atom numarası 17'dir. Klor, Cl sembolü ile gösterilir ve ametaldir.
Yeşilimsi sarı renkte bir gazdır.
Klorür iyonu yaşam için gereklidir. Eksi yüklü bir iyon olan klorür hücre sıvısında pozitif yüklü iyonları (özellikle potasyumu) dengelemek için kullanılır. Kanda da pozitif yüklü iyonları (özellikle sodyumu) dengeler.
Günlük klorür ihtiyacımızın çoğunu tuzdan karşılarız. Günlük 6 gram civarı tuz tüketmemize rağmen aslında ihtiyaç duyduğumuz tuz bunun yarısı kadardır.
Doğada saf hâlde bulunmaz, bileşikler içinde bulunur. Çoğunlukla tuz yataklarından elde edilir. Sodyum klorür kolay çözünen bir tuz olduğu için suyla karışıp deniz ve okyanuslarda birikir. Şimdi tuz yatağı olarak gördüğümüz maden ve göller, buharlaşan eski denizlerin kalıntılarıdır.
Zehirli bir gazdır.
Birinci Dünya Savaşı sırasında kimyasal silah olarak kullanıldı.
Bakterileri de öldürdüğü için içme suyu ve yüzme havuzu suları için dezenfektan olarak kullanılır.
Her yıl üretilen klorun %20'si PVC (polivinil klorür) üretiminde kullanılır. PVC pencere pervazı, elektrik yalıtımı, su borusu gibi farklı kullanım alanları olan çok amaçlı, polimer türü bir malzemedir.
Klorun bir diğer kullanım alanı da organik kimyadır. İlaçlardaki etken maddelerin %85'inin üretiminde klor veya klorlu bileşikler kullanılır.
Eskiden klor, kuru temizleme işlemlerinde yararlanılan karbon tetraklorür yapımında ve kloroform adında bir anestezik üretiminde yaygın olarak kullanılırdı. Ne var ki bu kimyasal maddelerin karaciğere ciddi hasarlar verdiği anlaşılınca kullanımları kısıtlanıp kontrol altına alındı.
18. Argon (Ar)

Argon, periyodik tablonun 3. periyodunun 18. grubunda yer alan bir elementtir. Argonun atom numarası 18'dir. Argon, Ar sembolü ile gösterilir ve soy gazdır.
Argon %0,94 ile atmosferde en yaygın bulunan üçüncü gazdır.
Argon; renksiz, kokusuz ve diğer bileşiklerle hiçbir şekilde tepkimeye girmeyen bir gazdır. Genellikle etkileşimsiz bir atmosfer oluşturmada kullanılır. Titanyum ve kimyasal tepkimelere girmeye istekli diğer elementlerin elde edilmesinde argondan faydalanılır.
Kaynak yapılan bölgenin oksitlenmesini engellemek için kaynak tabancalarında kullanılır.
Üzerinden akım geçtiğinde ışık yayan ince tellerin (filaman) oksijenle tepkimeye girip aşınmasını engellemek üzere akkor lambalarda kullanılır.
Floresan ve enerji tasarruflu lambalarda genellikle argon gazı bulunur. Lamba yakıldığında gazdan elektrik akımı geçer ve morötesi ışık yayılır. Lambanın içindeki kaplama malzemesi bu morötesi ışığı parlak görünür ışığa dönüştürür.
Çift katmanlı camları olan yalıtımlı pencerelerde katmanların arasında argon gazı bulunur. Bazı arabaların lastiklerinde de argon bulunabilir. Bu sayede lastik korunur ve tekerlek gürültüsünün önüne geçilir.
19. Potasyum (K)

Potasyum, periyodik tablonun 4. periyodunun 1. grubunda yer alan bir elementtir. Potasyumun atom numarası 19'dur. Potasyum, K sembolü ile gösterilir ve metaldir.
Yaşam için olmazsa olmaz elementlerdendir. Bütün hücrelerde potasyum bulunur. Sıvı ve elektrolit dengesini sağlar.
Potasyum bakımından zengin gıdalar muz, sardalya, fındık, kuru üzüm, patates, çikolata ve çözülebilir kahvedir.
Bitkiler önemli potasyum kaynaklarıdır, potasyumu doğrudan topraktan alırlar. Her yıl hasat yapılan tarım arazilerinde toprağa potasyumlu gübreler karıştırmak gerekir.
Okyanuslarda potasyum tuzları da vardır ancak sodyum tuzlarına oranla bu tuzların miktarı çok düşüktür.
Doğal olarak oluşan potasyum-40 izotopu radyoaktiftir. Radyoaktivitesi yüksek olmamasına rağmen insanlardaki genetik mutasyonun doğal nedenlerinden biri olabilir.
En önemli kullanım alanı gübre sanayiidir. Nitrat, karbonat, klorür, bromür, siyanür ve sülfat iyonlarıyla oluşturduğu bileşikler de hayli önemlidir.
Potasyum karbonat cam üretiminde, potasyum hidroksit deterjan ve sıvı sabun yapımında, potasyum klorür ise ilaç yapımında ve serumlarda kullanılır.
20.Kalsiyum (Ca)

Kalsiyum, periyodik tablonun 4. periyodunun 2. grubunda yer alan bir elementtir. Kalsiyumun atom numarası 20'dir. Kalsiyum, Ca sembolü ile gösterilir ve metaldir.
Bütün canlılar için özellikle de kemikler ve dişlerin sağlıklı gelişimi için gereklidir. Kemiklerin temel bileşenlerinden biri kalsiyum fosfattır. Ortalama bir insanda 1 kg civarı kalsiyum bulunur.
Özellikle kadın ve çocukların kalsiyum açısından zengin gıdalar tüketmesi tavsiye edilir. Bu gıdalar arasında süt ve süt ürünleri, yapraklı yeşil sebzeler, balık, kuru yemiş ve çeşitli çekirdekler sayılabilir.
Doğada saf hâlde bulunmaz ancak yaygın olarak kireç taşı, alçı taşı, apatit gibi minerallerin içinde bulunur.
Toryum ve uranyum gibi metallerin elde edilmesinde kalsiyumdan yararlanılır. Ayrıca alüminyum, berilyum, bakır, kurşun ve magnezyum ile alaşımlar oluşturur.
Kalsiyum karbonat bazlı kireç taşları inşaatlarda doğrudan ve işlendikten sonra çimento olarak kullanılır.
Kalsiyum sülfat bazlı alçı taşı (jips) kayaçlarından üretilen alçılar hem inşaat malzemesi olarak hem de kırık tedavisinde kemiği sabitlemek üzere atel olarak kullanılır.
21. Skandiyum (Sc)

Skandiyum, periyodik tablonun 4. periyodunun 3. grubunda yer alan bir elementtir. Skandiyumun atom numarası 21'dir. Skandiyum, Sc sembolü ile gösterilir ve metaldir.
Kansere neden olduğu düşünülse de bu görüş henüz ispat edilebilmiş değil.
Skandiyuma yeryüzünün çok farklı coğrafyalarında rastlanır. 800'den fazla mineralde çok az miktarlarda bulunur. Özellikle İskandinavya'da bulunan çok nadir bir mineral olan tortveititin temel bileşenlerindendir.
Genellikle bilimsel araştırmalarda kullanılır. Bununla birlikte yoğunluğu neredeyse alüminyum kadar düşük ve kaynama noktası alüminyuma göre çok daha yüksek olduğu için alüminyumla oluşturduğu alaşımlar savaş uçaklarında, profesyonel bisiklet iskeletlerinde ve bazı diğer spor ekipmanlarında kullanılır.
Skandiyum iyodür, cıva buharlı lambalarda gün ışığına yakın renk vermesi için kullanılır. Gece vakti veya iç mekânlarda çekim yapılırken gün ışığı etkisi oluşturmada bu lambalardan faydalanılır.
Radyoaktif skandiyum-46 izotopu petrol rafinelerinde çeşitli kırılma hareketlerinin takibi ve ayrıca yer altında bulunan tesisatlardaki sızıntıların tespiti için kullanılır.
22. Titanyum (Ti)

Titanyum, periyodik tablonun 4. periyodunun 4. grubunda yer alan bir elementtir. Titanyumun atom numarası 22'dir. Titanyum, Ti sembolü ile gösterilir ve metaldir.
Sert, parlak ve dayanıklı bir metaldir.
Zehirli değildir.
Çelik kadar sağlam olmasına rağmen yoğunluğu çelikten düşüktür. Bu yüzden alüminyum, molibden ve demir gibi pek çok metalle alaşımı yapılır. Yüksek sıcaklıklara dayanıklı olan, yoğunluğu az bu materyaller uçaklar, uzay araçları ve füzelerde kullanılır. Bununla birlikte dizüstü bilgisayarlar, bisikletler ve koltuk değneklerinde de kullanılırlar.
Paslanmaya karşı dirençli olduğu için enerji santrallerinin boru sistemlerinde, gemilerin gövdesinde, denizaltılarda ve tuzlu suya maruz kalan diğer yapılarda kullanılır.
Titanyum metali kemikle fiziksel olarak uyumlu olduğu için ortopedik uygulamalarda ve implant diş tedavisi gibi alanlarda kullanılır.
Titanyumun en geniş kullanım alanı titanyum dioksit biçimindedir. Ev boyaları, resim boyaları, plastikler, emaye ve kâğıtlarda beyaz renk vermesi için kullanılan etkili bir kaplama malzemesidir. Kızılötesi ışınımı yansıttığı için ısının görüşü zorlaştırdığı Güneş gözlemevlerinde kullanılır. Titanyum dioksit morötesi ışığın cildimize ulaşmasını engellediğinden güneş kremlerinde kullanılır.
23.Vanadyum (V)

Vanadyum, periyodik tablonun 4. periyodunun 5. grubunda yer alan bir elementtir. Vanadyumun atom numarası 23'dir. Vanadyum, V sembolü ile gösterilir ve metaldir.
İnsanlar da dâhil olmak üzere bazı canlılar için hayati önem taşır ancak çok az miktarda alınması yeterlidir. Örneğin günlük 0,01 mg vanadyum ihtiyacımızı fazlasıyla karşılar.
Vanadyum içeren birtakım bileşikler zehirli etki gösterebilir.
Dünya genelinde üretilen vanadyumun %80'i çelik üretiminde katkı maddesi olarak kullanılır. Vanadyum-çelik alaşımları hayli sağlamdır. Bu yüzden zırh kaplamalarında, otomobillerin motor aksamlarında kullanılırlar. %1 vanadyum ve %1 krom karıştırılarak çelik darbeye ve titreşime dayanıklı hale getirilir. Nötron soğurma özelliği düşük olduğundan nükleer reaktörlerde vanadyumlu alaşımlar kullanılır.
Vanadyum (V) oksit gümüşi renktedir. Seramik ve camlara renk vermek için kullanılır. Ayrıca süperiletken mıknatıslarda da kullanılır.
24. Krom (Cr)

Krom, periyodik tablonun 4. periyodunun 6. grubunda yer alan bir elementtir. Kromun atom numarası 24'dir. Krom, Cr sembolü ile gösterilir ve metaldir.
Kromlu bileşikler parlak yeşil, sarı, kırmızı ve turuncu renk verici maddeler olarak kullanılır. Yakut kırmızı rengini kromdan alır, kromlu camların zümrüt yeşili rengi olur.
Vücutta glikozun kullanılmasını sağladığı için insanlar için hayati önem taşır. Yüksek miktarda alınması zehirler. Günde 1 miligram alınması yeterlidir. Buğday rüşeymi ve böbrek krom açısından zengindir.
Krom, çeliği sertleştirmek ve paslanmaz çelik üretmek için kullanılır.
Krom gümüşi renkte parlak bir metal olduğu için çelik krom kaplama ile parlatılır. Otomobillerde ve çeşitli banyo gereçlerinde de krom kaplama yapılabilir.
Derinin işlenmesinde krom kullanılır ancak zehirli olduğu için buna bir alternatif bulunmaya çalışılıyor.
25.Manganez (Mn)

Manganez, periyodik tablonun 4. periyodunun 7. grubunda yer alan bir elementtir. Manganezin atom numarası 25'dir. Manganez, Mn sembolü ile gösterilir ve metaldir.
Manganez saf metal hâlinde kullanılamayacak kadar kırılgandır. Ancak çelik gibi alaşımlarda manganez bulunur. Dayanıklılığını, işlenebilirliğini ve sağlamlığını artırmak için çeliğe manganez eklenir. Alüminyum, antimon ve bakırla hayli manyetik bir alaşım oluşturur.
Manganez tüm canlılar için hayati önem taşır. Çeşitli enzimlerin yapısında manganez bulunur. Örneğin fotosentez sırasında su moleküllerinden oksijen üretilmesi sürecinde rol alan enzimde dört manganez atomu vardır.
Okyanus tabanlarında nodüller (temel olarak demir ve manganez oksitlerden oluşan, ancak içinde bakır, nikel, kobalt bulunan ceviz büyüklüğünde katı birikintiler) hâlinde bulunabilir.
Bazı topraklar manganez bakımından fakir olduğu için yetiştirilen bitkilerin manganezli gübrelerle desteklenmesi gerekir. Bununla birlikte otlayan hayvanların yemine de manganez karıştırılır.
İnsan vücudunda yaklaşık 12 miligram manganez bulunur. Kuru yemiş, tam tahıllı gevrek, buğday kepeği, çay ve maydanoz gibi gıdalardan günlük yaklaşık 4 miligram manganez alırız. Manganez kemiklere sertlik verir ve manganez eksikliği kemikleri kırılgan hâle getirir. Ayrıca B1 vitamininin vücutta işlenebilmesi için de manganez gereklidir.
Manganez (IV) oksit, içeriğindeki demir yüzünden yeşil renkte olan camları saydamlaştırmak için kullanılır.
Manganez sülfat, mantar öldürücü kimyasal maddelerde kullanılır. Manganez (II) oksit ise gübre ve seramiklerin üretiminde kullanılır.
Büyük oranda manganez (IV) oksit içeren piroluzit minarelleri yaklaşık 30.000 yıl önce mağara duvarlarına resim çizmek için kullanıldı.
26. Demir (Fe)

Demir, periyodik tablonun 4. periyodunun 8. grubunda yer alan bir elementtir.Demirinatom numarası 26'dir.Demir, Fe sembolü ile gösterilir ve metaldir.
Demir, yer kabuğunda en yaygın bulunan ikinci metal ve dördüncü elementtir.
Dünya'nın çekirdeği büyük oranda demirden oluşur ve önemli miktarda (yaklaşık %4 oranında) nikel içerir.
Yaşam için gerekli bir elementtir ve zehirli değildir. İnsan vücudunda ortalama 4 gram demir bulunur ve bunun önemli bir bölümü kandaki hemoglobin moleküllerindedir. Hemoglobin, oksijeni ciğerlerimizden hücrelere taşır. Her gün en az 10-18 miligram demir almamız gerekir. Demir eksikliği anemiye neden olabilir.
Karaciğer, böbrek, pekmez, kakao ve meyan kökü gibi besinlerde fazlaca demir vardır.
Mısır'da MÖ 3500'lü yıllardan kalma demir nesneler bulunduysa da bileşimlerindeki demir oranı bunların Dünya'ya çarpan gök taşlarından üretildiğini gösteriyor. Hititlerin MÖ 1500 civarında demiri ilk eriten medeniyet olduğu düşünülüyor. Bu yeni ve dayanıklı metal Hititlere ekonomik ve politik güç kazandırmış ve böylece Demir Devri başlamıştır. Demirin çeşitli alaşımlarının farklı özelliklerde olduğu o dönemlerde de dikkat çekmişti.
Farklı demir alaşımları üzerine ilk kitap 1722'de René Antoine Ferchault de Réaumur tarafından yazıldı. Bu kitapta yazar, içerdiği karbon oranının demiri nasıl etkilediği üzerinde durur.
Tarihte bir başka önemli dönüm noktası olan Sanayi Devrimi de demire bağlı olarak gelişti.
Demir kolayca paslanmasına rağmen en önemli metaldir. Günümüzde işlenen metallerin %90'ı demirdir.
Demirin çoğu çelik hâline getirilir ve inşaatlarda kullanılır. Demirin çeşitli metallerle bir araya gelmesiyle farklı çeşitlerde çelik üretilir. Bunların en yaygını karbon çeliğidir.
Nikel, krom, vanadyum, tungsten, manganez gibi metallerle üretilen alaşımlar hayli sağlam olur ve işlenmeleri kolaylaşır. Köprülerden elektrikli aygıtlara, bisikletlerden kesici aletlere pek çok alanda kullanılırlar.
Demir döküm %3-%5 oranında karbon içerir ve boru, valf ve pompa üretiminde kullanılır. Çelik gibi sağlam olmasa da daha ucuz olduğu için tercih edilebilir.
Demirden ve demir içeren çeşitli alaşım ve bileşiklerden mıknatıs üretilebilir.
Amonyak üretiminde katalizör (tepkimenin daha hızlı gerçekleşmesini sağlayan ancak kendisi tepkimede harcanmayan maddeler) olarak demirden yararlanılır.
Akaryakıt üretiminde de kullanılır.
27. Kobalt (Co)

Kobalt, periyodik tablonun 4. periyodunun 9. grubunda yer alan bir elementtir.Kobaltınatom numarası 27'dir. Kobalt, Co sembolü ile gösterilir ve metaldir.
MÖ 1361-1352 yılları arasında hüküm süren Mısır Firavunu Tutankamon'un tabutunda kobaltla renklendirilmiş küçük mavi bir cam obje bulundu. Kobaltın bu tarihten önce bile Çin'de porselen yapımı için kullanıldığı biliniyor.
Kobalt hayati önem taşıyan bir elementtir, B12 vitamininin önemli bir bileşenidir. Vücudumuzda yalnızca 1 miligram bulunur ancak eksikliği önemli hastalıklara yol açabilir. Mineral eksikliklerini gidermek için belirli hayvanların yemlerine kobalt tuzları eklenebilir. Ne var ki yüksek dozda alınması hâlinde kansere yol açabilir.
Okyanus tabanlarında nodüller (temel olarak demir ve manganez oksitlerden oluşan, ancak içinde bakır, nikel, kobalt bulunan ceviz büyüklüğünde katı birikintiler) hâlinde bulunabilir.
Kobalt da demir gibi manyetik hâle getirilebilir ve mıknatıs yapımında kullanılabilir.
Alüminyum ve nikel alaşımları özellikle güçlü mıknatıslar elde etmek için kullanılır.
Erime noktası yüksek, dolayısıyla ısıya dayanıklı olduğu için jet türbinlerinde ve gaz türbin jeneratörlerinde kullanılır.
Gümüşi mavi rengi, sağlamlığı ve paslanmaya direnci nedeniyle kaplama malzemesi olarak da tercih edilir.
Boya, porselen, cam, çömlek ve emayelere mavi renk vermek amacıyla yüzyıllardır kobalt tuzları kullanılır.
Kobalt-60 izotopu radyoaktiftir, önemli bir gama ışını kaynağıdır ve kanser tedavisinde (radyoterapide) kullanılır. Bazı ülkelerde yiyecekleri ışınla steril hâle getirmek ve uzun süre saklamak amacıyla da kullanılır.
28. Nikel (Ni)

Nikel, periyodik tablonun 4. periyodunun 10. grubunda yer alan bir elementtir.Nikelinatom numarası 28'dir.Nikel, Ni sembolü ile gösterilir ve metaldir.
Bitkilerin gelişimine katkı sağlayabilir ve bazı canlı türleri için hayati önem taşır. Ne var ki nikel içeren bazı bileşiklerin dumanının solunması kansere neden olabilir. Bazı insanlarda da nikel alerjisi vardır.
Nikelden tamamen kaçınmak neredeyse imkânsızdır. Besinlerimizle birlikte vücudumuza nikel alırız. Özellikle kuru fasulyede bulunur.
Nikelin azımsanamayacak bir miktarı Dünya'ya gök taşları ile ulaştı. Bunların en önemlilerinden biri milyonlarca yıl önce bugün Kanada sınırında bulunan Ontario'nun yakınlarına düştü. Dünya genelindeki nikelin yaklaşık %15'i bu bölgeden elde edilir.
Gök taşlarında demir ve nikel bulunur. Eski çağlarda insanlar bu alaşımı demirin paslanmayan üstün bir çeşidi olarak görüp kullandılar. Hatta Perulular bu metali gümüş zannediyordu.
Nikel paslanmadığından diğer metaller paslanmamaları için nikel ile kaplanır. Paslanmaz çelik yapımında da nikel kullanılır. Az miktarda silisyum, manganez ve demir de içeren nikel-krom alaşımları ısıya dayanıklı ve paslanmaz oldukları için tost makineleri ve elektrikli fırınlarda kullanılır.
Bir bakır-nikel alaşımı, tuzlu suyu tatlı suya çeviren tuz giderme tesislerinde kullanılır.
Nikel çeliği zırh kaplamalarında kullanılır.
Batarya ve pillerde de kullanılır. Şarj edilebilir nikel-kadmiyum piller ve hibrit araçlarda kullanılan nikel-metal hidrür piller bunlara örnektir.
Nikel uzun yıllardır bozuk paralarda da kullanılıyor. ABD'de "nikel" denilen 5 sentlik bozuk paranın %25'i nikel, %75'i bakırdır.
Doymamış yağların doymuş yağlara dönüştürülmesinde katalizör (kimyasal tepkimelerin daha hızlı gerçekleşmesini sağlayan ancak kendisi tepkimede harcanmayan maddeler) olarak nikel de kullanılır.
Cam üretimi sırasında nikel eklenmesi cama yeşil renk verir.
29. Bakır (Cu)

Bakır, periyodik tablonun 4. periyodunun 11. grubunda yer alan bir elementtir.Bakırınatom numarası 29'dir.Bakır, Cu sembolü ile gösterilir ve metaldir.
Bakır insanlar tarafından işlenen ilk metaldir. Kalayla bakırın karıştırılarak daha sağlam olan tuncun elde edilmesiyle Tunç Devri başladı.
Yaşamsal açıdan önemli bir elementtir. Yetişkin bir insanda enzimlerin hücrede enerji taşımasına yardımcı olması için günde 1,2 miligram bakıra ihtiyaç duyulur. Fazla miktarda alınması zehirli etkiye yol açabilir.
Vücutlarında oksijeni taşımak için kanda bulunan hemoglobin molekülündeki demiri kullanan memelilerin aksine, bazı kabuklu hayvanlarda aynı iş için bakırlı bileşikler kullanılır.
Para dökümlerinde bakır ile birlikte altın ve gümüş de kullanılırdı ancak bu metaller arasında en kıymetsizi bakır olduğu için bakır paralar daha yaygındı. Günümüzdeki bozuk paralarda da bakır kullanımı yaygındır.
Hem ısıyı hem de elektriği çok iyi ilettiği ve kolayca şekillendirilebildiği için bakırın en büyük kullanım alanı elektrikli aletler ve tellerdir. Bununla birlikte inşaatlarda ve sanayide kullanılan makinelerde de bakır vardır.
Tarım ilacı olarak ve su arıtmada algleri öldürmek için bakır sülfat kullanılır.
Bakırlı bileşikler şeker tespiti için yapılan kimyasal testlerde kullanılır.
30. Çinko (Zn)

Çinko, periyodik tablonun 4. periyodunun 12. grubunda yer alan bir elementtir.Çinkonunatom numarası 30'dir.Çinko, Zn sembolü ile gösterilir ve metaldir.
Çinko yaşam için gerekli elementlerden biridir. 20'den fazla enzim için gereklidir. İnsan vücudunda yaklaşık 2,5 gram çinko vardır ve yiyeceklerden günde yaklaşık 15 miligram çinko alırız. Çinko bakımından zengin gıdalar ringa balığı, sığır eti, kuzu eti, ay çekirdeği ve peynirdir. Fazla miktarda alınması kansere sebep olabilir.
Çinko genellikle diğer metallerle birlikte kullanılır. Örneğin demirin paslanmasını önler. Bu yüzden en önemli kullanım alanlarından biri dökümlerdir. Bunlar otomobil parçalarında, elektrik ve donanım endüstrisinde kullanılır.
Çinko oksit boya, kauçuk, ilaç, plastik, mürekkep, sabun, pil, kumaş ve elektrik malzemesi üretiminde kullanılır.
Çinko sülfür parlak renkli boyalarda, floresan lambalarda ve X-ışını ekranlarda kullanılır.
31. Galyum (Ga)

Galyum, periyodik tablonun 4. periyodunun 13. grubunda yer alan bir elementtir.Galyumunatom numarası 31'dir.Galyum, Ga sembolü ile gösterilir ve metaldir.
Zehirli değildir.
Galyum arsenür (GaAs) yarı iletken özellikte bir malzemedir ve elektronik endüstrisinde kullanılır. Mars keşif aracındaki güneş panellerinde galyum arsenür vardır. Pek çok yarı iletkenin önemli bir bileşenidir.
Elektriği ışığa dönüştürebildiğinden LED'lerde kullanılır.
Galyum nitrür de yarı iletken özellikte bir malzemedir. Blu-ray (mavi ışın) teknolojisinde, cep telefonlarında, mavi ve yeşil LED lambalarda ve dokunmatik yüzeylerdeki basınç algılayıcılarda kullanılır.
Metallerin çoğu ile alaşım yapabilir. Özellikle erime sıcaklığı düşük alaşımlarda kullanılır.
32.Germanyum (Ge)

Germanyum, periyodik tablonun 4. periyodunun 14. grubunda yer alan bir elementtir.Germanyumunatom numarası 32'dir.Germanyum, Ge sembolü ile gösterilir ve yarı metaldir.
Yarı metaldir.
Zehirli değildir. Bazı germanyumlu bileşiklerin, insanlar için çok zehirli değilken, belirli bakterilere karşı güçlü etki göstermesi nedeniyle ilaç endüstrisinde kullanılabileceği düşünülüyor.
Yarı iletken özellik gösteren saf germanyum eskiden arsenik, galyum ve başka elementlerle birlikte transistör üretiminde kullanılırdı. Günümüzde yarı iletken özellik gösteren başka malzemeler germanyumun yerini aldı.
Germanyum oksidin kırılma indisi yüksek olduğu için geniş açılı kamera mercekleri ve mikroskop lenslerinde kullanılır. Günümüzde germanyumun en geniş kullanım alanı merceklerdir.
Gümüşe çok az miktarda germanyum eklendiğinde kararması önlenir.
Hem germanyum hem de germanyum oksit kızılötesi ışınımı geçirdiklerinden kızılötesi tayfölçerlerde kullanılır.
33. Arsenik (As)

Arsenik, periyodik tablonun 4. periyodunun 15. grubunda yer alan bir elementtir.Arseniğinatom numarası 33'dir.Arsenik, As sembolü ile gösterilir ve yarı metaldir.
Yarı metaldir.
En bilinen zehirlerden biridir. Küçük dozlarda bile zehirli etkiye sahiptir ve kansere neden olabilir. Vücuda alındığında saçtaki atomlara bağlanır, bu yüzden birinin arsenikle zehirlenip zehirlenmediğini anlamak için saçı analiz edilebilir.
Fare zehri ve böcek ilaçlarının içinde bulunsa da kullanımı sıkı denetlenir.
Arseniğin tıbbi kullanım alanları da vardır. İngiltere'de Kraliçe Viktorya döneminde (1837-1901) Dr. Fowler'ın Çözeltisi adı verilen bir tonik (suda çözünmüş potasyum arsenat) mucize ilaç olarak kullanılıyordu. Bu toniği kullanan kişiler arasında tanınmış yazar Charles Dickens da vardı. Günümüzde arsenik bileşikleri hastalıkları önlemek ve kilo almalarını kolaylaştırmak üzere kümes hayvanlarının yemlerine karıştırılıyor.
Karideste yüksek miktarda organoarsenik bileşikleri (karbon-arsenik bağı içeren bileşikler) vardır. Organoarsenikler sağlığa zararlı değildir.
Pek çok yarı iletken malzemenin önemli bir bileşenidir. Elektronik endüstrisinde silisyum yerine galyum arsenür kullanılır. Mars keşif aracındaki güneş panellerinde de galyum arsenür vardır.
Arsenikli bileşenlerle özel camlar üretilebilir ve ahşapların uzun süre bozulmadan kalması sağlanabilir.
Arsenik Eski Mısırlılar tarafından metalleri parlatmak amacıyla kullanılıyordu. 1500'lü yıllarda Çin'de arsenikli bileşiklerin zehirli olduğu ve çeltik tarımında böcek ilacı olarak kullanılabileceği biliniyordu.
34.Selenyum (Se)

Selenyum, periyodik tablonun 4. periyodunun 16. grubunda yer alan bir elementtir.Selenyumunatom numarası 34'dir.Selenyum, Se sembolü ile gösterilir ve ametaldir.
Deri yoluyla da emilebilen selenyum kötü kokusu nedeniyle ağız kokusuna yol açar.
Yarı metaldir. İki hâlde bulunabilir: gümüşi metal ya da kırmızı toz.
İnsanlar da dâhil birtakım canlılar için hayati önem taşır. Vücudumuzda yaklaşık 14 miligram selenyum vardır. Her bir hücremizde bir milyondan fazla selenyum atomu bulunur.
Eksikliği sağlık sorunlarına yol açabilirken fazlası tehlikelidir. Kansere yol açabilir, embriyo ya da fetüsün gelişimini olumsuz etkileyebilir.
Selenyumdan en çok cam üretiminde katkı maddesi olarak yararlanılır. Bazı selenyum bileşikleri camı şeffaflaştırırken bazı bileşikleri kırmızı renk verir. Seramik, boya ve plastik renklendirmede selenyumdan faydalanılır.
Paslanmaz çeliğin bileşiminde selenyum bulunur.
Hem fotovoltaik (ışığı elektriğe dönüştürme) hem de fotoiletken (üzerine düşen ışık miktarı arttıkça elektriksel direncinin düşmesi) özelliklere sahip olduğu için ışık gözelerinde, güneş gözelerinde ve fotokopi makinelerinde kullanılır.
Aynı zamanda alternatif akımı (AC) doğru akıma (DC) dönüştürebildiği için akım doğrultucularda da yaygın olarak kullanılır.
Kepeğe neden olan saç derisi mantarını zehirlediği için bazı kepeğe karşı şampuanlara eklenir.
35. Brom (Br)

Brom, periyodik tablonun 4. periyodunun 17. grubunda yer alan bir elementtir.Bromunatom numarası 35'dir.Brom, Br sembolü ile gösterilir ve ametaldir.
Az miktarda da olsa tüm canlılarda bulunur. Gözlerle teması hâlinde kaşıntı ve kızarıklık, boğaza kaçması durumunda öksürük ve cilde teması hâlinde ağrılı yaralara yol açabilir.
Tarımda kullanılan kimyasal maddelerde, boyalarda, böcek öldürücü ilaçlarda ve birtakım ilaçlarda kullanılır. Çevreye verdiği zarardan ötürü kullanımını azaltmaya yönelik çalışmalar vardır. Bununla birlikte gün geçtikçe yeni kullanım alanları bulunuyor.
Alevlerin yayılmasını önlediği için mobilyalarda, elektronik aletlerin dış katmanında ve kumaşlarda kullanılır. Kurşunlu benzinin kullanıldığı zamanlarda erken ateşlenmeyi önlemek amacıyla yakıtlara bromlu bir bileşik (C2H4Br2) eklenirdi.
Karbon-brom bağları içeren organik bileşikler yangın söndürücülerde kullanılır.
Eski tip fotoğraf makineleri ve kameralarda kullanılan filmlerde gümüş bromür bulunurdu.
36. Kripton (Kr)

Kripton, periyodik tablonun 4. periyodunun 18. grubunda yer alan bir elementtir.Kriptonunatom numarası 36'dir.Kripton, Kr sembolü ile gösterilir ve asal gazdır.
Havadaki gazdan argon gazını ayrıştırmayı başaran Sir William Ramsay ve Morris Travers periyodik tabloda yeni bir element grubu olduğunu düşünerek ayrıştırma sürecini devam ettirmeye karar verdiler. Bu sürecin sonunda argondan daha ağır bir gaz bulacaklarını öngörüyorlardı ve düşündükleri gerçekleşti. 1898'de kriptonu keşfettiler.
Kripton gazı renksiz ve kokusuzdur.
Enerji tasarruflu ampullerde ve saniyede 69 kare ve daha yüksek hızla yapılan fotoğraf çekimlerinde kullanılan ışıklarda bulunur.
Periyodik tablonun soy gazlar grubundaki kütle numarası daha küçük elementlere göre tepkimeye girmeye daha isteklidir. Flor ile tepkimeye girdiğinde bazı lazerlerde kullanılan kripton florür oluşur.
Metre, 1960'tan 1983'e dek kripton-86 izotopunun yaydığı bir dalganın boyunun 1.650.763,73 katı olarak tanımlanıyordu. 1983'ten sonra metrenin tanımı ışık hızına göre yapılmaya başlandı.
37.Rubidyum (Rb)

Rubidyum, periyodik tablonun 5. periyodunun 1. grubunda yer alan bir elementtir.Rubidyumunatom numarası 37'dir.Rubidyum,Rb sembolü ile gösterilir ve metaldir.
Havai fişeklere mor renk vermek için bazen rubidyum nitrat kullanılır.
Bilimsel araştırmalar dışında kullanım alanı kısıtlıdır. Vakum tüplerindeki oksijen kalıntılarını temizlemede, ayrıca özel camların ve ışığa duyarlı hücrelerin üretiminde kullanılır.
Çok kolay iyonlaştığı (iyonlaşma bir atomun ya da molekülün elektron alarak ya da vererek elektriksel olarak yüklü hale geçmesidir) için uzay araçlarının iyon motorlarında kullanılması düşünüldüyse de sezyum elementinin daha etkili olduğunun anlaşılması nedeniyle bu amaçla kullanılmadı.
38.Stronsiyum (Sr)

Stronsiyum, periyodik tablonun 5. periyodunun 2. grubunda yer alan bir elementtir.Stronsiyumunatom numarası 38'dir.Stronsiyum,Sr sembolü ile gösterilir ve metaldir.
Havai fişek ve işaret fişeklerine verdiği parlak kırmızı renk ile bilinir.
Bazı derin deniz canlılarının kabuklarında bulunur ve bazı mercan kayaları için hayati önem taşır. İnsanlar için biyolojik bir etkisi yoktur ve zehirli değildir. Kalsiyumla benzeştiği için vücudumuzda kemikler tarafından emilir.
Seramik yapılı (ferrit) mıknatısların üretiminde ve çinkonun saflaştırılmasında kullanılır.
Günümüzde karanlıkta parıldayan boya ve plastiklerde stronsiyum alüminat bulunur. Gün ışığında soğurdukları ışığı sonrasında yavaşça yayarlar.
Stronsiyum-90 izotopu radyoaktiftir ve nükleer reaktörlerde yan ürün olarak ortaya çıkar. Nükleer atıklarda da bulunur. Yarılanma ömrü 28 yıldır. Yapısı kalsiyuma benzediği için kemiklerde kalsiyum yerine emilir ve kemik iliğinin işlevini yerine getirememesine ve kansere yol açabilir. Nükleer patlamalarla açığa çıkar ve nükleer enerji santrali kazalarında çevreye yayılabilir. Özellikle kemik gelişimi devam eden çocukları ve gençleri olumsuz etkiler.
Bilinen en iyi yüksek enerjili beta ışını yayan elementtir. Uzay araçları için enerji üretimi, uzaktan kontrol edilebilen hava istasyonları ve navigasyon şamandıralarında kullanılır.
Kalınlık ölçümü yapan cihazlarda ve kâğıt ya da plastik ambalajlama makinelerinde statik enerjiyi gidermek için de kullanılır.
Hassas dişler için üretilen diş macunlarında stronsiyumlu bir bileşik kullanılır.
39.İtriyum (Y)

İtriyum, periyodik tablonun 5. periyodunun 3. grubunda yer alan bir elementtir.İtriyumunatom numarası 39'dir.İtriyum,Y sembolü ile gösterilir ve metaldir.
Gümüşi beyaz renkte, yumuşak bir metaldir.
Periyodik tabloda bir üst sıradaki skandiyum elementi ve lantanitlerle (periyodik tabloda atom numarası 57-71 arasındaki elementler) birlikte nadir toprak metallerini oluştururlar.
Nadir toprak metalleri arasında seryumdan sonra yer kabuğunda en bol bulunan elementtir.
Floresan aydınlatmalarda ve televizyonlarda kırmızı ışık kaynağı olarak kullanılır.
Başka bir önemli kullanım alanı süperiletken (sıcaklık belirli bir değerin altına düştüğünde bir malzemenin elektrik direncinin tamamen sıfır olması) malzeme üretimidir. Örneğin itriyum baryum bakır oksit malzemesi yüksek sıcaklık süperiletkeni olarak sınıflandırılır.
İtriyum-90 izotopu bazı kanser türlerinin tedavisinde kullanılan ilaçların içinde yer alır.
40.Zirkonyum (Zr)

Zirkonyum, periyodik tablonun 5. periyodunun 4. grubunda yer alan bir elementtir.Zirkonyumunatom numarası 40'dir.Zirkonyum,Zr sembolü ile gösterilir ve metaldir.
Gümüşi renkte, dayanıklı ve dövülerek şekillendirilebilen bir metaldir.
Zehirli değildir.
Hava ve sulu çözeltilerle temas ettiğinde yüzeyinde hemen bir zirkonyum oksit tabakası oluşur. Bu tabaka zirkonyumun korozyona (kimyasal olarak aşınmaya) karşı dirençli olmasını sağlar.
Yer kabuğunda bulunan ve ekonomik değeri olan mineralleri zirkon ve baddeleyittir.
En yaygın kullanıldığı alan nükleer enerji üretimidir. Hem nötronları soğurmaması hem de aşınmaya karşı dirençli olması sebebiyle nükleer yakıt çubuklarını içeren tüplerin imalatında kaplama malzemesi olarak zirkonyumlu alaşımlar kullanılır.
Zirkonyum oksit (ZrO2) seramik endüstrisinde malzemelerin dayanıklılığını artırmak için kullanılır.
41.Niyobyum (Nb)

Niyobyum, periyodik tablonun 5. periyodunun 5. grubunda yer alan bir elementtir. Niyobyumun atom numarası 41'dir. Niyobyum, Nb sembolü ile gösterilir ve metaldir.
Gümüşi renkte, yumuşak ve dövülerek şekillendirilebilen bir metaldir.
Yüzeyinde oluşan oksit tabakası niyobyumun korozyona (kimyasal olarak aşınmaya) karşı dirençli olmasını sağlar.
Yer kabuğunda tantal, demir ve manganez elementleri ile birlikte oluşturduğu minerallerin içinde bulunur.
Süperiletken özellik gösterir. Bu nedenle parçacık hızlandırıcılardaki (örneğin CERN'deki Büyük Hadron Çarpıştırıcı'da) ve manyetik rezonans görüntüleme (MRI) cihazlarındaki süperiletken mıknatıslarda kullanılır.
Niyobyum oksit, kırılma indisini artırmak amacıyla cama eklenir. Böylece daha ince merceklerden yapılan gözlük camları üretilebilir.
Niyobyum ve zirkonyum alaşımları zehirli olmadığından ve bağışıklık sisteminin tepki vermesine neden olmadığından dişçilikte dolgu malzemesi olarak ve vücuda yerleştirilen implantların üretiminde kullanılır.
42.Molibden (Mo)

Molibden, periyodik tablonun 5. periyodunun 6. grubunda yer alan bir elementtir. Molibdenin atom numarası 42'dir. Molibden, Mo sembolü ile gösterilir ve metaldir.
Parlak gümüşi renkte, sert ve erime noktası çok yüksek bir metaldir.
Bitkilerde ve hayvanlarda bazı biyokimyasal süreçlerin gerçekleşmesi için gerekli bir elementtir. Örneğin molibden içeren enzimler atmosferdeki azot gazının amonyağa dönüşmesini sağlayan tepkimenin daha hızlı gerçekleşmesinde katalizör görevi yapar. Bu süreç canlılarda azot içeren bileşiklerin biyolojik olarak sentezlenmesi için gereklidir.
Canlılarda çok az miktarda bulunur. Ancak fazlası zehirlidir.
Yer kabuğunda yaygın olarak molibdenit minerali şeklinde bulunur.
Malzemelerin yüksek sıcaklığa ve korozyona (kimyasal olarak aşınmaya) karşı dirençli olmasını sağlamak, sertliklerini, elektrik ve ısı iletkenliklerini artırmak amacıyla alaşımlara eklenir.
Kimya endüstrisinde katalizör (kimyasal tepkimelerin daha hızlı gerçekleşmesini sağlayan ancak kendisi tepkimede harcanmayan maddelerdir) olarak kullanılır. Özellikle benzin ve dizel gibi petrol ürünlerinin çevreye daha az zarar vermesini sağlamak amacıyla petrol ürünlerindeki kükürdün uzaklaştırılmasında kullanılır.
43.Teknetyum (Tc)

Teknetyum, periyodik tablonun 5. periyodunun 7. grubunda yer alan bir elementtir. Teknetyumun atom numarası 43'tür. Teknetyum, Tc sembolü ile gösterilir ve metaldir.
Periyodik tablodaki yapay olarak üretilen ilk elementtir. Bütün izotopları radyoaktiftir.
İzotoplarının yarı ömürleri görece kısa olduğundan (En uzun yarı ömürlü izotopu olan teknetyum-97'nin yarı ömrü yaklaşık 4,2 milyon yıldır.) yer kabuğunda neredeyse hiç bulunmaz. Ancak 1962'de Gabon Cumhuriyeti'ndeki uranyum yataklarındaki cevherlerde teknetyumun bulunduğu anlaşıldı.
Teknetyum-99 izotopu, yakıt olarak uranyumun kullanıldığı nükleer reaktörlerde nükleer fisyon tepkimesi sonucunda açığa çıkan ürünlerden biridir.
Teknetyum-99m yapay bir radyoaktif element izotopu olması nedeniyle tiroit hastalıklarının teşhisinde kullanılır. Ayrıca teknetyum-99m özel bileşikleri ile kanserli doku ve hücrelerin görüntülenmesinde kullanılır.
44.Rutenyum (Ru)

Rutenyum, periyodik tablonun 5. periyodunun 8. grubunda yer alan bir elementtir. Rutenyumun atom numarası 44'tür. Rutenyum, Ru sembolü ile gösterilir ve metaldir.
Sert ve kırılgan bir metaldir.
Yer kabuğunda genellikle platin grubu metallerle (rutenyum, rodyum, paladyum, osmiyum, iridyum ve platin) birlikte oluşturduğu cevherler şeklinde bulunur.
Yakıt olarak uranyumun ve plütonyumun kullanıldığı nükleer reaktörlerde nükleer fisyon tepkimesi sonucu oluşan ürünlerden biridir.
Paladyum ve platin alaşımlarının sertliğini artırmak amacıyla kullanılır.
Kimya endüstrisinde katalizör (kimyasal tepkimelerin daha hızlı gerçekleşmesini sağlayan ancak kendisi tepkimede harcanmayan maddeler) olarak kullanılır.
Rutenyum içeren bileşiklerin kullanıldığı güneş gözelerinin geliştirilmesine yönelik araştırmalar devam ediyor. Bu sayede günümüzde kullanılan güneş gözelerine alternatif olabilecek düşük maliyetli bir malzeme üretilebileceği düşünülüyor.
45.Rodyum (Rh)

Rodyum, periyodik tablonun 5. periyodunun 9. grubunda yer alan bir elementtir. Rodyumun atom numarası 45'tir. Rodyum, Rh sembolü ile gösterilir ve metaldir.
Beyaz-mavisimsi renkte, sert, dövülerek şekillendirilebilen bir metaldir.
Kuvvetli asitlere karşı dirençlidir. Aynı zamanda hava ve su ile kolayca tepkimeye girmez.
Doğada rodyum-103 izotopu şeklinde bulunur.
Doğada çoğunlukla diğer platin grubu metallerle (rutenyum, rodyum, paladyum, osmiyum, iridyum ve platin) birlikte oluşturduğu cevherler şeklinde bulunur.
Motorlu araçlarda kullanılan katalitik konvertörlerin en önemli bileşenidir. Bu cihaz, motorlu araçlarda yakıtın yanması sonucu oluşan azot oksit bileşiklerinin zararlı olmayan azot gazına ve oksijen gazına dönüştüğü kimyasal tepkimenin daha hızlı gerçekleşmesini sağlar.
Beyaz altının dış görünümünü iyileştirmek ve gümüşün hava ile tepkimeye girerek kararmasını engellemek amacıyla kaplama malzemesi olarak kullanılır.
46.Paladyum (Pd)

Paladyum, periyodik tablonun 5. periyodunun 10. grubunda yer alan bir elementtir. Paladyumun atom numarası 46'dır. Paladyum, Pd sembolü ile gösterilir ve metaldir.
Parlak, gümüşi beyaz renkte bir metaldir.
Dövülerek kolayca şekillendirilebilir.
Platin grubu metaller (rutenyum, rodyum, paladyum, osmiyum, iridyum ve platin) arasında erime noktası ve yoğunluğu en düşük olandır.
Platin grubu metaller arasında yer kabuğunda en bol bulunandır. Yer kabuğunda tek başına ya da başka elementlerle oluşturduğu minerallerin içinde bulunabilir.
En önemli kullanım alanı otomotiv endüstrisidir. Motorlu araçlardaki katalitik konvertörlerde kullanılır. Yakıtın yanması sonucu oluşan zararlı maddelerin (örneğin hidrokarbonların, karbonmonoksidin ve azot oksit bileşiklerinin) suya, karbondiokside ve azot gazına dönüştüğü kimyasal tepkimelerin daha hızlı gerçekleşmesini sağlar.
Kendi hacminin 900 katı kadar hidrojen gazı soğurabilir. Metal ısıtıldığında hidrojen gazı tekrar serbest kalabilir. Bu özelliği sayesinde hidrojen gazının saflaştırılmasında kullanılır.
47. Gümüş (Ag)

Gümüş, periyodik tablonun 5. periyodunun 11. grubunda yer alan bir elementtir. Gümüşün atom numarası 47'dir. Gümüş, Ag sembolü ile gösterilir ve metaldir.
Gümüşi renkte, görece yumuşak ve dövülerek şekillendirilebilen bir metaldir.
Altın ve platin grubu metalleri ile birlikte değerli metaller olarak isimlendirilirler.
Işığı yansıtma kapasitesi, elektrik ve ısı iletkenliği en yüksek metaldir.
Yer kabuğunda tek başına ya da başka elementlerle oluşturduğu minerallerin (örneğin kurşun, bakır, kadmiyum cevherleri) içinde bulunabilir.
Yer kabuğunda nadir bulunan elementlerden biri olmasına rağmen doğal olarak oluşan birçok mineralde bulunur.
Gümüşün ekonomik değeri olan minerallerinden biri arjantittir (gümüş sülfür).
Havadaki kükürt içeren maddelerle tepkimeye girdiğinde yüzeyinde siyah renkli gümüş sülfür bileşiği oluşur ve zamanla kararır.
Çok eski zamanlardan beri madeni para, süs eşyası, çeşitli aletler ve mücevher yapımında kullanılır.
Kimya endüstrisinde etilenin etilen okside ve formaldehide dönüştürülmesinde katalizör (kimyasal tepkimelerin daha hızlı gerçekleşmesini sağlayan ancak kendisi tepkimede harcanmayan maddeler) olarak kullanılır.
48.Kadmiyum (Cd)

Kadmiyum, periyodik tablonun 5. periyodunun 12. grubunda yer alan bir elementtir. Kadmiyumun atom numarası 48'dir. Kadmiyum, Cd sembolü ile gösterilir ve metaldir.
Yer kabuğunda grenokit (kadmiyum sülfür) mineralinde ve çinko cevherlerinde bulunur.
Gümüşi beyaz renkte, mavimsi parıltıları olan, yumuşak bir metaldir.
İnsan vücudunda çok az miktarda bulunur. Ancak fazlası zehirlidir. Kansere ve anne karnındaki bebeklerde gelişim problemlerine neden olabilir.
Nemli havada oksitlenerek kahverengindeki kadmiyum okside dönüşür.
Kükürtle tepkimeye girmesi sonucu oluşan kadmiyum sülfür bileşiği parlak sarı renktedir ve boya pigmenti olarak kullanılır.
Büyük kısmı şarj edilebilir kadmiyum-nikel pillerde kullanılır.
Nötron soğurabildiğinden nükleer reaktörlerde nükleer fisyon tepkimelerinin hızının kontrol edilmesinde kullanılan kontrol çubuklarının üretiminde kullanılır.
49.İndiyum (In)

İndiyum, periyodik tablonun 5. periyodunun 13. grubunda yer alan bir elementtir. İndiyumun atom numarası 49'dur. İndiyum, In sembolü ile gösterilir ve metaldir.
Gümüşi renkte, yumuşak bir metaldir. Havada ve suda kararlı yapıdadır.
Birkaç miligramdan daha fazla tüketilirse zehirli olabilir ve fetüs gelişimini etkileyebilir.
Doğada en nadir bulunan madenlerden biridir. Her ne kadar sadece indiyum çıkarılan madenler olsa da genelde çinko mineralleriyle ya da demir, kurşun ve bakır cevherleriyle birlikte bulunur.
Büyük çoğunluğu elektriği iyi ilettiği, cama güçlü bir biçimde tutunduğu ve ışığı geçirdiği için dokunmatik ekranlarda, düz ekran televizyonlarda ve güneş gözelerinde kullanılan indiyum kalay oksidin üretiminde kullanılır.
Uzun binaların camlarında ayna yüzey olarak ve kaynak gözlüğünde koruyucu film tabakası olarak kullanılır.
Sürtünme özelliği düşük olduğundan dolayı Formula 1 araçlarının bilyalı rulmanlarını kaplamak için kullanılır.
İndiyum nitrür, indiyum fosfür ve indiyum antimonit yarı iletkendir, transistör ve mikroçiplerde kullanılırlar.
50. Kalay (Sn)

Kalay, periyodik tablonun 5. periyodunun 14. grubunda yer alan bir elementtir. Kalayın atom numarası 50'dir. Kalay, Sn sembolü ile gösterilir ve metaldir.
Yumuşak ve esnek bir metaldir. 13 °C'nin altındaki sıcaklıklarda toz hâline gelir.
Zehirli değildir. Ancak kalay içeren organik bileşikler zehirli olabilir ve dikkatli kullanılmalıdır.
Başlıca kaynağı, kasiterit (kalay oksit) cevherleridir. Çin, Tayland ve Endonezya'yı içine alan "kalay kuşağı"nın yanı sıra Peru, Bolivya ve Brezilya'da da çıkarılır.
Çeşitli metaller, aşınmaya karşı kalayla kaplanır. Örneğin konserve kutuları çeliğin kalayla kaplanmasıyla üretilir.
Niyobyum ve kalay içeren bir alaşım, süperiletken mıknatıslarda kullanılır.
Birçok pencere camı, düz bir yüzey oluşturmak için, erimiş camın erimiş kalayın üzerine dökülmesiyle üretilir.
Bazı kalay bileşikleri gemilerde ve botlarda kabuklu deniz canlılarına karşı koruyucu boya olarak kullanılır. Ancak çok düşük miktarda kullanılsa bile deniz canlılarına zarar verdiği için bu bileşiklerin kullanımı pek çok ülkede yasaktır.
51.Antimon (Sb)

Antimon, periyodik tablonun 5. periyodunun 15. grubunda yer alan bir elementtir. Antimonun atom numarası 51'dir. Antimon, Sb sembolü ile gösterilir ve yarı metaldir.
Yarı metaldir. Metal formundayken gümüşi renkte, sert ve kırılgandır.
Antimon ve antimon içeren pek çok bileşik zehirlidir.
Doğada az bulunur, ancak antimon içeren yüzden fazla mineral vardır. Doğada çoğunlukla antimon (III) sülfür bileşikleri hâlinde bulunur. Ayrıca doğal metalik ya da alaşımlar hâlinde de bulunabilir.
%88'i Çin'de üretilir. Antimon üreten diğer ülkeler Bolivya, Rusya ve Tacikistan'dır.
Elektronik sanayiinde kızılötesi dedektörler ve diyotlar gibi yarı iletken aygıtların yapımında kullanılır.
Sertliklerini artırmak için kurşun ya da diğer metallerle karıştırılarak alaşımları üretilir. Kurşun-antimon alaşımı pillerde kullanılır. Ayrıca antimonlu bileşikler parlamayı önleyici materyallerde, boyalarda, emayelerde, camlarda ve çömlekçilikte kullanılır.
52. Tellür (Te)

Tellür, periyodik tablonun 5. periyodunun 16. grubunda yer alan bir elementtir. Tellürün atom numarası 52'dir. Tellür, Te sembolü ile gösterilir ve yarı metaldir.
Yarı metaldir. Genellikle gri renkli toz hâlinde elde edilir.
Çok zehirli ve teratojeniktir (embriyo gelişimini engelleyici). Çok az miktarının bile solunması ağızda sarımsak kokusuna benzer bir koku oluşmasına neden olur.
Yer kabuğunda bulunma oranı sadece milyonda 0,001'dir. Tellür içeren mineraller arasında kalaverit, silvanit ve tellürit vardır. Ayrıca az miktarda da olsa doğada metalik formda da bulunur. Ticari olarak ihtiyaç duyulan tellür, bakırın elektronik rafinesi sırasında anot çamurundan elde edilir. Bu çamurların içinde yaklaşık %8 oranında tellür bulunur.
İçine tellür eklenen kurşun, asitlere karşı daha dirençli hâle gelir, sertliği artar.
Bakırın ve paslanmaz çeliğin işlenebilirliğini artırmak için kullanılır.
Kauçuğu sertleştirmekte, camları ve seramikleri renklendirmekte, güneş gözelerinde, yeniden yazılabilir CD ve DVD'lerin yanı sıra yağ arıtımında katalizör (kimyasal tepkimelerin daha hızlı gerçekleşmesini sağlayan ancak kendisi tepkimede harcanmayan maddeler) olarak da kullanılır.
53. İyot (I)

İyot, periyodik tablonun 5. periyodunun 17. grubunda yer alan bir elementtir. İyotun atom numarası 53'tür. İyot, I sembolü ile gösterilir ve ametaldir.
Siyah, parlak, kristal yapılı bir katıdır. Isıtıldığında mor renkli bir buhara dönüşür.
İnsan vücudunda 20 miligrama kadar iyot bulunabilir, çoğunluğu tiroit bezindedir. Tükettiğimiz gıdalarda normalde yeterli miktarda iyot vardır. Günlük 0,1 miligram iyot almamız gerekir. İyot eksikliği, tiroit bezinin şişmesine ve guatr hastalığının oluşmasına sebep olur.
Deniz suyunda iyotlu bileşikler vardır. Ancak deniz yosunları tarafından soğuruldukları için sulardaki iyot oranı milyonda 0,05'ten düşüktür. Geçmişte iyot, deniz yosunlarından elde edilirdi. Günümüzdeki ana kaynağıysa iyot içeren minerallerdir.
İlk ticari kullanım alanı fotoğrafçılıktı. Günümüzdeyse pek çok alanda kullanılıyor. İyot LCD ekranlar için polarize filtre yapımında, iyot tuzlarıysa tıbbi ilaçlar ve dezenfektanlarda, mürekkep ve boyalarda, hayvan yemlerinde ve fotoğrafçılıkla ilgili kimyasal maddelerin üretiminde kullanılır.
Eksikliği tiroit bezlerini olumsuz etkilediği için çok az miktarda sofra tuzlarına eklenir.
Radyoaktif iyot-131 izotopu kanserli tiroit bezlerinin tedavisinde kullanılır.
54. Ksenon (Xe)

Ksenon, periyodik tablonun 5. periyodunun 18. grubunda yer alan bir elementtir. Ksenonun atom numarası 54'tür. Ksenon, Xe sembolü ile gösterilir ve soy gazdır.
Kokusuz ve renksiz bir gazdır. Kimyasal tepkimelere girmeye karşı çok isteksizdir, soy gazdır.
Kendisi zehirsizdir ancak ksenon içeren bileşikler çok zehirlidir.
Ticari olarak ihtiyaç duyulan ksenon, sıvılaştırılmış havadan elde edilir. Atmosferde hacimce milyonda 0,086 oranında ksenon bulunur.
Bazı özel ışık kaynaklarında kullanılır. Ksenon atomları, voltaj uygulanarak uyarıldıklarında mavi ışık yayar. Fotoğrafçılar tarafından kullanılan yüksek hızlı flaş lambalarında, cilt bronzlaştırıcı lambalarda, gıda endüstrisindeki bakteri yok edici lambalarda ksenon kullanılır.
İyon itki sistemlerinde, bazı uydularda ve uzay araçlarını yörüngede tutmada kullanılır.
55.Sezyum (Cs)

Sezyum, periyodik tablonun 6. periyodunun 1. grubunda yer alan bir elementtir. Sezyumun atom numarası 55'tir. Sezyum, Cs sembolü ile gösterilir ve metaldir.
Altın renginde, yumuşak bir metaldir. Havayla hızla tepkimeye girer, suyla tepkimeye girdiğinde patlar.
Polüsit ve lepidolit madenlerinde bulunur. Ticari olarak ihtiyaç duyulan sezyum, lityumun yan ürünü olarak elde edilir.
Sezyumun en önemli kullanım alanlarından biri atom saatleridir. Sezyum atom saatleri; internetin, mobil telefon ağlarının ve GPS sistemlerinin düzgün çalışması açısından hayli önemlidir. Bazı sezyum saatleri on beş milyon yılda sadece bir saniye sapar.
56. Baryum (Ba)

Baryum, periyodik tablonun 6. periyodunun 2. grubunda yer alan bir elementtir. Baryumun atom numarası 56'dır. Baryum, Ba sembolü ile gösterilir ve metaldir.
Gümüşi renkte, yumuşak bir metaldir. Hava ve su ile temas ettiği anda matlaşır.
Baryumun yanı sıra suda ve asitte çözünen baryum bileşikleri zehirlidir. Ancak tıbbi görüntülemelerden önce içilen baryum sülfat suda çözünmediği için zararsızdır.
Sadece özel bir alg türünde baryum sülfat bulunur.
Baryum doğada diğer elementlerle bir arada bulunur. Ana kaynağı barit (baryum sülfat) ve viterit (baryum karbonat) madenleridir.
Baryum karbonat geçmişte fare zehri olarak kullanılırdı.
Baryum nitrat, havai fişeklere yeşil bir renk verir. Çoğunlukla yağ ve gaz kuyularında sondaj sıvısı olarak kullanılır. Ayrıca boya ve cam yapımında da kullanılır.
57.Lantan (La)

Lantan, periyodik tablonun 6. periyodunun lantanitler grubunda yer alan 1. elementtir. Lantanın atom numarası 57'dir. Lantan, La sembolü ile gösterilir ve metaldir.
Gümüşi beyaz renkte, yumuşak bir metaldir. Havayla temas ettiği anda matlaşan ve kolay yanan bir metaldir.
Hem elementin kendisi hem de bileşikleri orta düzeyde zehirlidir.
Ticari bir kullanımı yoktur. Fakat alaşımları farklı yerlerde kullanılır. Lantan-nikel alaşımı hidrojen gazının depolanmasında kullanılır.
Nadir toprak mineralleri olan monazit ve bastnazit madenlerinde bulunur.
58.Seryum (Ce)

Seryum, periyodik tablonun 6. periyodunun lantanitler grubunda yer alan 2. elementtir.. Seryumun atom numarası 58'dir. Seryum, Ce sembolü ile gösterilir ve metaldir.
Gri bir metaldir ve çok çabuk karardığı için kullanım alanı çok azdır. Su ile tepkimeye girer ve ısıtıldığında tutuşur.
Seryum, sertçe vurulduğunda kıvılcım çıkardığı için, çakmak taşlarındaki mishmetal alaşımın en önemli bileşenlerinden biridir.
Seryum (III) oksit kendi kendini temizleyen fırınlarda yiyecek kalıntılarının artmasını engellemek için kullanılır.
Yakıtın daha iyi yanmasını sağlayacağı ve böylece egzoz emisyonunu düşüreceği tahmin edildiği için dizel yakıtlara eklenmesi konusunda araştırmalar yapılıyor.
Zehirsiz bir bileşik olan seryum sülfür kırmızı rengi nedeniyle pigment olarak kullanılır.
Seryum düz ekranlı televizyonlarda, düşük enerjili lambalarda ve projektörlerde de kullanılır.
Doğada en fazla bulunan lantanit seryumdur.
59.Praseodim (Pr)

Praseodim, periyodik tablonun 6. periyodunun lantanitler grubunda yer alan3. elementtir. Praseodimin atom numarası 59'dur. Praseodim, Pr sembolü ile gösterilir ve metaldir.
Düşük düzeyde zehirlidir.
Gümüşi renkte, yumuşak bir metaldir.
Pek çok metalle alaşım oluşturur. Magnezyumla oluşturduğu alaşım uçak motorlarında kullanılır.
Çakmaklardaki çakmak taşlarında bulunan mishmetalde yaklaşık %5 oranında praseodim vardır.
Kalıcı mıknatıslarda da praseodim bulunur.
Diğer lantanitlere benzer şekilde, stüdyo ışıklandırmalarında ve projektörlerde kullanılır.
Emaye ve camları renklendirmede, özellikle de sarı renk vermede praseodimin tuzları kullanılır. Sarı ışığı ve kızılötesi ışımayı engellediği için cam üreticileri ve kaynak yapanların taktığı koruyucu gözlüklerdeki camlarda, neodimle birlikte praseodim kullanılır.
60.Neodim (Nd)

Neodim, periyodik tablonun 6. periyodunun lantanitler grubunda yer alan 4. elementtir. Neodimin atom numarası 60'tır. Neodim, Nd sembolü ile gösterilir ve metaldir.
Gümüşi beyaz renkte bir metaldir. Havayla temas ettiğinde matlaşır.
Orta düzeyde zehirlidir.
En önemli kullanım alanı çok güçlü kalıcı mıknatıs üretimidir. Demir ve bor ile oluşturduğu alaşımları içeren bu güçlü mıknatıslar sayesinde aralarında cep telefonu, mikrofon, hoparlör ve elektronik müzik aletlerinin de bulunduğu pek çok elektronik cihazın küçültmesi mümkün oldu. Bu mıknatıslar araba sileceklerinde ve rüzgâr türbinlerinde de kullanılır.
Cam üreticileri ve kaynak yapanların taktığı koruyucu gözlüklerdeki camlarda praseodim ile birlikte neodim bulunur.
Cama mor, kızıl ve gri renk vermek için kullanılır. Kızılötesi ışınları engelleyip bronzlaştırıcı morötesi ışınları geçirdiği için bronzlaşma kabinlerindeki camlarda da kullanılır.
Neodim camlar kullanılarak üretilen lazerlerden işaretçilerde, göz ameliyatlarında ve deri kanseri tedavisinde yararlanılır.
61.Prometyum (Pm)

Prometyum, periyodik tablonun 6. periyodunun lantanitler grubunda yer alan5. elementtir. Prometyumun atom numarası 61'dir. Prometyum, Pm sembolü ile gösterilir ve metaldir.
Radyoaktif bir metaldir. Daha çok bilimsel araştırmalarda kullanılır. Ayrıca nükleer bataryalarda çok az miktarda prometyum bulunur. Aşağı yukarı bir raptiye boyutunda olan bu bataryalar kalp pillerinde, güdümlü füzelerde ve radyolarda kullanılır. Prometyumun radyoaktif bozunmasından fosforlu maddelerin ışık açığa çıkarmasını sağlamak için yararlanılır. Bu ışık güneş gözesi tarafından elektriğe dönüştürülür.
Prometyumdan ölçüm cihazlarında X-ışını ve radyoaktivite kaynağı olarak da yararlanılır.
62.Samaryum (Sm)

Samaryum, periyodik tablonun 6. periyodunun lantanitler grubunda yer alan 6. elementtir. Samaryumun atom numarası 62'dir. Samaryum, Sm sembolü ile gösterilir ve metaldir.
Gümüşi beyaz renkte bir metaldir.
Düşük düzeyde zehirlidir.
Samaryum-kobalt mıknatıslar, demir mıknatıslardan çok daha güçlüdür. Yüksek sıcaklıklarda bile manyetik etkilerini koruyabilmelerinden dolayı mikrodalga uygulamalarında kullanılırlar. Kulaklık gibi elektronik aletlerin küçülebilmesi bu mıknatısların kullanım alanlarının genişletilmesi ile mümkün oldu. Ancak artık neodim mıknatıslar, samaryum-kobalt mıknatıslardan daha yaygın bir biçimde kullanılıyor.
Optik lazerlerde kullanılan kalsiyum klorür kristallerine samaryum eklenir.
Kızılötesi ışınları soğuran camlarda ve nükleer reaktörlerdeki nötron soğurucularda kullanılır.
Samaryum oksit, cam ve seramik yapımında kullanılır.
Diğer lantanitlere benzer şekilde, stüdyo ışıklandırmalarında ve projektörlerde kullanılır.
63.Evropiyum (Eu)

Evropiyum, periyodik tablonun 6. periyodunun lantanitler grubunda yer alan 7. elementtir. Evropiyumun atom numarası 63'tür. Evropiyum, Eu sembolü ile gösterilir ve metaldir.
Düşük düzeyde zehirlidir.
Gümüşi renkte, suyla tepkimeye giren, hızla matlaşan, yumuşak bir metaldir.
Evropiyum, euro banknotlarının basımında kullanılır. Banknotlar morötesi ışığa maruz bırakıldıklarında evropiyum kırmızı ışık yayar. Bu sayede paranın sahte olup olmadığı anlaşılabilir.
Enerji tasarruflu lambalarda çok az miktarda evropiyum vardır. Bu sayede mavi ışığın kırmızı ışıkla dengelenmesi ve daha doğal ışık üretilmesi sağlanır.
Nötron soğurmada çok iyi olduğu için nükleer reaktörlerdeki kontrol mekanizmalarında kullanılır.
Evropiyum katkılı plastikler lazer malzemesi olarak kullanılır.
64.Gadolinyum (Gd)

Gadolinyum,periyodik tablonun 6. periyodunun lantanitler grubunda yer alan 8. elementtir. Gadolinyumun atom numarası 64'tür. Gadolinyum, Gd sembolü ile gösterilir ve metaldir.
Düşük düzeyde zehirlidir.
Çok az miktarlarda bile olsa içerisinde gadolinyum bulunan alaşımların özellikleri iyileşir. İçinde demir ve krom bulunan alaşımlara sadece %1 oranında gadolinyum eklendiğinde bile yüksek sıcaklıklara ve oksitlenmeye karşı daha dayanıklı hâle gelirler. Mıknatıs, elektronik devre elemanları ve veri saklama disklerinin yapımında kullanılan alaşımlarda da bulunur.
Gadolinyumun bileşikleri manyetik rezonans görüntüleme (MRI) sistemlerinde, özellikle de kanserli hücrelerin tespit edilmesinde kullanılır.
Nötron soğurma kapasitesi çok yüksek olduğu için nükleer reaktörlerin çekirdeklerinde de kullanılır.
65.Terbiyum (Tb)

Terbiyum, periyodik tablonun 6. periyodunun lantanitler grubunda yer alan 9. elementtir.Terbiyumun atom numarası 65'tir.Terbiyum, Tb sembolü ile gösterilir ve metalidir.
Gümüşi renkte, yumuşak bir metaldir.
Düşük düzeyde zehirlidir.
Enerji tasarruflu lambalarda ve cıva lambalarında kullanılır.
X-ray cihazlarında hastayı ışınlara daha kısa süre maruz bırakarak yüksek çözünürlüklü görüntü elde etmede kullanılır.
Terbiyum tuzları lazer cihazlarında kullanılır.
Terbiyum, disprosyum ve demir içeren bir alaşım, manyetik alan etkisiyle uzayıp kısalabilir. Bu özelliği sayesinde düz zeminlere yerleştirilebilen hoparlörlerin icadına zemin hazırladı.
66.Disprosyum (Dy)

Disprosyum, periyodik tablonun 6. periyodunun lantanitler grubunda yer alan 10. elementtir. Disprosyumun atom numarası 66'dır.Disprosyum, Dy sembolü ile gösterilir ve metalidir.
Düşük düzeyde zehirlidir.
Su ve hava ile kolayca tepkimeye girdiğinden saf hâldeyken neredeyse kullanılmaz.
Yüksek sıcaklıklarda manyetik özelliklerini koruyabildiği için asıl kullanım alanı, neodim temelli mıknatısların üretildiği alaşımlardır. Motor ve jeneratörlerde kullanılan mıknatısların ısıya dayanıklı olması gerekir. Bu mıknatıslar rüzgâr türbinleri ve elektrikli aletlerde kullanıldığı için disprosyum ihtiyacı gün geçtikçe artıyor.
Disprosyum iyodür tuzu, halojen lambalarda kullanılır ve parlak beyaz ışık yayar.
Disprosyum oksit ve nikel içeren bir tür sermet (seramik ve metal içeren bir tür kompozit malzeme) nükleer reaktörlerin kontrol mekanizmalarında kullanılır.
Nötronları kolayca soğurur, uzunca bir süre nötron bombardımanına maruz kalsa da şeklini korur.
67.Holmiyum (Ho)

Holmiyum, periyodik tablonun 6. periyodunun lantanitler grubunda yer alan11. elementtir. Holmiyumunatom numarası 67'dir.Holmiyum, Ho sembolü ile gösterilir ve metaldir.
Zehirli değildir.
Parlak, gümüşi renkte bir metaldir.
Nötronları soğurabildiği için nükleer reaktörlerdeki zincir tepkimeleri kontrol etmede yararlanılır.
Alaşımları mıknatıslarda kullanılır.
68. Erbiyum (Er)

Erbiyum, periyodik tablonun 6. periyodunun lantanitler grubunda yer alan 12. elementtir. Erbiyumunatom numarası 68'dir.Erbiyum, Er sembolü ile gösterilir ve metaldir.
Düşük düzeyde zehirlidir.
Su ile tepkimeye girdiği ve açık havada hızla matlaştığı için saf haldeyken neredeyse kullanılmaz.
Vanadyum gibi metallerle alaşım oluşturarak sertlik düzeylerini düşürür ve bu metallerin biçimlendirilmesini mümkün kılar.
Kızılötesi ışımayı soğurduğu için metal işçilerinin ve kaynak yapanların taktığı koruyucu gözlüklerdeki camlarda kullanılır.
Cama pembe bir ışıltı verir. Bu yüzden bazı güneş gözlüklerinde ve taklit mücevherlerde kullanılır.
Fiber optik kablolarla iletilen geniş bantlı sinyaller, cam elyafına erbiyum katılarak yükseltilir.
69. Tulyum (Tm)

Tulyum, periyodik tablonun 6. periyodunun lantanitler grubunda yer alan 13. elementtir.Tulyumunatom numarası 69'dur.Tulyum, Tm sembolü ile gösterilir ve metaldir.
Zehirli değildir.
Parlak, gümüşi renkte bir metaldir.
Nükleer reaktörde radyasyona maruz kalınca, X-ışını yayan bir izotopa dönüşür. Bu izotoptan tıbbi amaçlarla kullanılan taşınabilir X-ışını makinelerinin üretiminde yararlanılır. Ameliyatlarda kullanılan lazerlerde de tulyum bulunur.
70.İterbiyum (Yb)

İterbiyum, periyodik tablonun 6. periyodunun lantanitler grubunda yer alan 14. elementtir. İterbiyumunatom numarası 70'tir.İterbiyum, Yb sembolü ile gösterilir ve metaldir.
Düşük düzeyde zehirlidir.
Gümüşi renkte, yumuşak bir metaldir. Havayla temas ettiğinde yavaşça oksitlenir ve yüzeyinde koruyucu bir tabaka oluşturur.
Yer kabuğunda monazit mineralinde bulunur.
Gün geçtikçe iterbiyum için, veri saklama aygıtları ve ayarlanabilir lazerler başta olmak üzere, farklı kullanım alanları ortaya çıkıyor.
1841'de Carl Mosander seryadan (1803'te keşfedilen ve çeşitli oksitler içeren bir karışımdan) lantan ile birlikte didimiyumu ayrıştırıp bulduğu maddelerin yeni elementler olduklarını öne sürdükten sonra, 1794'te bulunan itriyumun da saf olmayabileceğini düşünerek ondan da yeni elementler ayrıştırabileceğini düşündü. 1843'te itriyumdan terbiyum oksit ve erbiyum oksidi ayrıştırmayı başardı. Bu elementler de diğer lantanitlerin bulunmasında rol oynadı. 1878'de Jean-Charles Galissard de Marignac erbiyumdan iterbiyum adını verdiği başka bir elementi ayrıştırmayı başardı. Ancak bunlar da saf değildi, bir yıl sonra da iterbiyumdan skandiyum, erbiyumdan ise tulyum ayrıştırıldı. 1907'de de iterbiyumdan lütesyum ayrıştırıldı.
71.Lütesyum (Lu)

Lütesyum, periyodik tablonun 6. periyodunun lantanitler grubunda yer alan 15. elementtir. Lütesyumunatom numarası 71'dir.Lütesyum, Lu sembolü ile gösterilir ve metaldir.
Gümüşi beyaz renkte, sert ve yoğun bir metaldir.
Düşük düzeyde zehirlidir.
Bilimsel araştırmalar dışında kullanım alanı çok azdır. Ticari kullanım alanlarından biri, petrol rafinerilerinde hidrokarbonları parçalamak için yararlanılan katalizörlerdir (kimyasal tepkimelerin daha hızlı gerçekleşmesini sağlayan ancak kendisi tepkimede harcanmayan maddeler).
72.Hafniyum (Hf)

Hafniyum, periyodik tablonun 6. periyodunun 4. grubunda yer alan bir elementtir.Hafniyumunatom numarası 72'dir.Hafniyum, Hf sembolü ile gösterilir ve metaldir.
Parlak, gümüşi renkte bir metaldir.
Periyodik tabloda aynı grupta bulunduğu zirkonyum elementinin altında yer alır. Hafniyumun kimyasal özellikleri zirkonyum ile benzerdir.
Toz hâldeki hafniyumun su ile tepkimeye girmesi sonucu yanıcı bir gaz olan hidrojen gazı açığa çıkar.
Yer kabuğundaki başlıca kaynağı zirkon cevheridir. Zirkon mineralinin (Temel bileşenleri zirkonyum, silisyum ve oksijen elementleridir.) içinde çok az miktarlarda bulunur.
Hafniyum, niyobyum, titanyum ve tungstenden elde edilen alaşımlar termal ve mekanik olarak dirençli malzemelerdir.
Nötron soğurma kapasitesi yüksek olduğu için nükleer reaktörlerde fisyon tepkimesini kontrol etmeye yarayan kontrol çubuklarının üretiminde kullanılır.
73.Tantal (Ta)

Tantal, periyodik tablonun 6. periyodunun 5. grubunda yer alan bir elementtir.Tantalınatom numarası 73'tür.Tantal, Ta sembolü ile gösterilir ve metaldir.
Gümüşi renkte bir metaldir.
Çok serttir, dayanıklıdır ve dövülerek şekillendirilebilir. Erime noktası yüksektir, korozyona (kimyasal olarak aşınmaya) karşı dirençlidir, ısıyı ve elektriği iyi iletir.
Yer kabuğunda nadiren saf metal hâlde bulunur. Çoğunlukla niyobyum ile birlikte oluşturduğu cevherler şeklinde bulunur.
İnsanlarda bağışıklık sisteminin tepki vermesine neden olmadığından vücuda yerleştirilen implantların ve protezlerin üretiminde kullanılır.
Geçmişte akkor lambalarda üzerinden akım geçtiğinde ışık yayan ince tellerin (filaman) üretiminde kullanılmıştı.
Bilgisayarlardan akıllı telefonlara elektronik cihazlarda bulunan kapasitörlerin üretiminde kullanılır.
Başka metallerle oluşturduğu alaşımlar hayli dayanıklıdır. Havacılıkta jet motorlarındaki türbin kanatçıklarının üretiminde kullanılır.
74.Tungsten (W)

Tungsten, periyodik tablonun 6. periyodunun 6. grubunda yer alan bir elementtir.Tungsteninatom numarası 74'tür. Tungsten, W sembolü ile gösterilir ve metaldir.
Parlak, gümüşi beyaz renkte bir metaldir.
Erime noktası en yüksek metaldir. Diğer metallerle oluşturduğu alaşımlar çok dayanıklıdır, korozyona (kimyasal olarak aşınmaya) karşı dirençlidir ve elektriği iyi iletir.
Yer kabuğunda nadir olarak bulunan elementlerdendir. Çoğunlukla şelit ve volframit cevherlerinden elde edilir. Doğada saf metal hâlde bulunmaz, diğer elementlerle oluşturduğu bileşikler şeklinde bulunur.
En çok akkor lambalarda üzerinden akım geçtiğinde ışık yayan ince tellerin (filaman) üretiminde kullanılır.
Yüksek sıcaklığa karşı dayanıklı olması nedeniyle motorlardaki türbin kanatçıklarının ve motor kapaklarının üretiminde kullanılır.
Tungstenin karbonla oluşturduğu tungsten karbür bileşiği, çok sert malzemeleri (örneğin sert metalleri ve kayaçları) kesmek ve delmek amacıyla kullanılan aletler ile tükenmez kalemlerin uçlarındaki bilyelerin ve dişçilikte dişleri kesmek için yararlanılan aletlerin üretimde kullanılır.
75.Renyum (Re)

Renyum, periyodik tablonun 6. periyodunun 7. grubunda yer alan bir elementtir.Renyumunatom numarası 75'tir.Renyum, Re sembolü ile gösterilir ve metaldir.
Renyum gümüşi beyaz renkte bir metaldir.
Yer kabuğunda en nadir bulunan elementlerden biridir. Doğada saf metal hâlde bulunmaz. Çoğunlukla molibdenit cevherlerinden elde edilir. 660 kilogram molibdenit cevherinden sadece 1 gram renyum elde edilebilir.
Erime noktası en yüksek elementlerden biridir. Renyum ve oluşturduğu alaşımlar çok yüksek sıcaklıklara dayanıklı olmaları nedeniyle savaş uçaklarındaki jet motorlarının türbin kanatçıklarının üretiminde kullanılır. Ayrıca petrokimya endüstrisinde kurşun içermeyen yüksek oktanlı petrol ürünlerinin elde edilmesinde katalizör (kimyasal tepkimelerin daha hızlı gerçekleşmesini sağlayan ancak kendisi tepkimede harcanmayan maddeler) olarak yararlanılır.
76.Osmiyum (Os)

Osmiyum, periyodik tablonun 6. periyodunun 8. grubunda yer alan bir elementtir.Osmiyumunatom numarası 76'dır.Osmiyum, Os sembolü ile gösterilir ve metaldir.
Gümüşi beyaz renkte sert ve kırılgan bir metaldir. Yoğunluğu en yüksek elementtir.
Oksijenle tepkimesi sonucu oluşan osmiyum tetraoksit bileşiği zehirli ve tahriş edicidir. Osmiyum tetraoksit erime sıcaklığının altında süblimleşir yani katı hâlden doğrudan gaz hâle geçer.
Yer kabuğunda nadir olarak bulunan elementlerden biridir.
Osmiyum dolma kalem uçlarının ve gramofon iğnelerinin yapımında kullanılır. Kimya endüstrisinde katalizör (kimyasal tepkimelerin daha hızlı gerçekleşmesini sağlayan ancak kendisi tepkimede harcanmayan maddelerdir) olarak yararlanılır.
77.İridyum (Ir)

İridyum, periyodik tablonun 6. periyodunun 9. grubunda yer alan bir elementtir.İridyumunatom numarası 77'dir.İridyum, Ir sembolü ile gösterilir ve metaldir.
Gümüşi beyaz renkte, sert ve kırılgan bir metaldir. Osmiyumdan sonraki en yoğun elementtir.
1803'te İngiliz kimyacı Smithson Tennant tarafından keşfedildi.
Yer kabuğunda en nadir bulunan kararlı elementlerden biridir. Doğada çok düşük oranda saf hâlde ve yaygın olarak osmiyumla oluşturduğu alaşımlar şeklinde bulunabilir. Yeryüzündeki iridyumun kaynağının Dünya'ya çarpan bir gök taşı olduğu tahmin ediliyor. Çünkü asteroitlerin yapısındaki iridyum oranı görece yüksektir. Jeolojik tarihlendirme çalışmaları, iridyumun yer kabuğunda yüksek oranda bulunduğu ince katmanın yaklaşık 65 milyon yıl önce oluştuğunu gösteriyor. Bazı bilim insanları Dünya'daki iridyumun kaynağı olan gök taşının dinozorların neslinin yok olmasına neden olan gök taşı ile aynı olduğunu düşünüyor.
Başka metallerle karıştırılmasıyla elde edilen alaşımlar farklı amaçlarla kullanılır. Örneğin iridyum-osmiyum alaşımı dolma kalem uçlarında, platin-iridyum alaşımı ise standart olarak belirlenen kilogram ölçü prototipinin üretiminde kullanılır.
78. Platin (Pt)

Platin, periyodik tablonun 6. periyodunun 10. grubunda yer alan bir elementtir.Platininatom numarası 78'dir. Platin, Pt sembolü ile gösterilir ve metaldir.
Parlak, gümüşi beyaz renkte bir metaldir.
Tepkimeye girmeye isteksiz bir element olduğundan korozyona (kimyasal olarak aşınmaya) ve yüksek sıcaklığa karşı dirençlidir.
Değerli bir metal olan platin altın gibi mücevher yapımında sıkça kullanılır.
Kimya endüstrisinde nitrik asit, sülfürik asit, gübre ve patlayıcı üretiminde katalizör (kimyasal tepkimelerin daha hızlı gerçekleşmesini sağlayan ancak kendisi tepkimede harcanmayan maddeler) olarak kullanılır.
Yakıt pillerinin verimliliğinin artırılmasında kullanılır.
79. Altın (Au)

Altın, periyodik tablonun 6. periyodunun 11. grubunda yer alan bir elementtir.Altının atom numarası 79'dur.Altın, Au sembolü ile gösterilir ve metaldir.
Sarı renkte bir metaldir.
Dövülerek kolayca şekillendirilebilir.
Altının insanlar tarafından çok eski zamanlardan beri kullanıldığı biliniyor. MÖ 1323'te ölen firavun Tutankamon'un mezarından çıkan maske altından yapılmıştı. Altın paralar ilk defa Anadolu'da Lidyalılar tarafından basıldı. Altın uluslararası bir ödeme aracı olarak hâlen kullanılıyor.
Çok eski zamanlardan beri insanlar tarafından süs eşyası olarak kullanılıyor.
Tepkimeye girmeye isteksiz bir element olduğundan korozyona (kimyasal olarak aşınmaya) karşı dirençli olması ve elektriği iyi iletmesi nedeniyle 20. yüzyılın sonundan itibaren endüstride kullanılmaya başlandı. Bilgisayarlarda, uzay araçlarında, elektronik cihazlarda ve uçak motorlarında kullanılır.
Nano ölçekteki altın parçacıkları endüstride katalizör (kimyasal tepkimelerin daha hızlı gerçekleşmesini sağlayan ancak kendisi tepkimede harcanmayan maddeler) olarak kullanılır.
80. Cıva (Hg)

Cıva, periyodik tablonun 6. periyodunun 12. grubunda yer alan bir elementtir.Cıvanın atom numarası 80'dir.Cıva, Hg sembolü ile gösterilir ve metaldir.
Parlak, gümüşi renkte bir metaldir.
Oda sıcaklığında sıvı hâlde bulunur. Isı iletkenliği düşüktür ancak elektriği iyi iletir. Cıvanın yoğunluğu yüksektir, 1 cm3cıva yaklaşık 13,5 gramdır.
Cıvanın yutulması, buharının solunması ve deri yoluyla soğurulması çok düşük miktarda da olsa sağlık açısından tehlikelidir. İnsanlar vücutlarındaki cıvayı çoğunlukla yedikleri balık ve kabuklu deniz ürünlerinden alır.
Çoğunlukla cıva sülfür (HgS) cevherlerinden elde edilir.
Bataryalarda, floresan aydınlatmalarda, termometre ve barometrelerde (basınçölçer), diş dolgu malzemesi olan amalgamlarda kullanılır. Ancak canlılar üzerindeki zehirlilik etkisi nedeniyle Dünya Sağlık Örgütü (WHO) tarafından cıvanın medikal malzemelerde ve ölçüm cihazlarındaki kullanımına 2020 yılına kadar aşamalı olarak son verilmesi çağrısı yapıldı.
81.Talyum (Tl)

Talyum, periyodik tablonun 6. periyodunun 13. grubunda yer alan bir elementtir. Talyumun atom numarası 81'dir. Talyum, Tl sembolü ile gösterilir ve metaldir.
Gümüşi beyaz renkte, çabuk matlaşabilen, yumuşak bir metaldir.
Aşırı zehirlidir. Buharı teratojenik (embriyo gelişimini engelleyici) ve kanserojendir. Vücutta potasyum ile yer değiştirip sinir sistemine etki edebilir.
Genellikle fotoelektrik göze yapımında kullanılır. Talyumlu bileşikler fare zehri, kırılma indisi yüksek ya da erime noktası düşük cam yapımında kullanılır.
Çoğunlukla bakır, çinko ve kurşun rafinelerinden yan ürün olarak elde edilir. Okyanus tabanlarındaki magnezyum nodüllerinde (temel olarak demir ve manganez oksitlerden oluşan ancak içinde bakır, nikel, kobalt bulunan ceviz büyüklüğünde katı birikintiler) de bulunur.
82. Kurşun (Pb)

Kurşun, periyodik tablonun 6. periyodunun 14. grubunda yer alan bir elementtir. Kurşunun atom numarası 82'dir. Kurşun, Pb sembolü ile gösterilir ve metaldir.
Keşfi antik dönemlere kadar uzanır.
Gümüşi renkte, mat ve kaplama özelliği olan, yumuşak bir metaldir.
Zehirli, teratojenik (embriyo gelişimini engelleyici) ve kanserojendir. Vücutta birikerek ciddi sağlık problemlerine neden olabilir. Zararlı olduğu için günümüzde sırlı çömlek, böcek ilacı, saç boyası gibi alanlarda kullanılması yasaktır.
Kolayca levha hâline getirilebilir. Kolay işlenebilir ve paslanmaz yapısı sayesinde Roma döneminden bu yana boru, kalay alaşımı ve boya yapımında kullanılır.
Araba akülerinde, mühimmat üretiminde, kablo yalıtımında, radyasyondan korunma amacıyla yararlanılan kalkanlarda ve bazı lehimlerde kullanılır.
İngiltere'de kullanılan kurşunun en az %40'ı atık pil ve boruların geri dönüştürülmesiyle elde edilir.
83. Bizmut (Bi)

Bizmut, periyodik tablonun 6. periyodunun 15. grubunda yer alan bir elementtir. Bizmutun atom numarası 83'tür. Bizmut, Bi sembolü ile gösterilir ve metaldir.
Tarih öncesi zamanlardan beri kullanıldığı biliniyor. Ancak uzun süre kurşun, antimon ve kalay ile karıştırıldı. 1753'te bizmutun farklı bir element olduğu Claude François Geoffroy tarafından keşfedildi.
Yüksek yoğunluklu, gümüşi ve pembeye çalan renkte bir metaldir.
Zehirli değildir.
Doğada saf ya da alaşımlar hâlinde bulunur. Kurşun, bakır, kalay, gümüş ve altının arıtılması sırasında da yan ürün olarak elde edilir.
Aşırı kırılgan yapısından dolayı farklı metallerle karıştırılarak kullanılır. Kalay veya kadmiyumla oluşturduğu alaşımların erime sıcaklığı düşüktür. Bu yüzden yangın dedektörü, yangın söndürücüsü, elektrik sigortası ve lehimlemede kullanılır.
84.Polonyum (Po)

Polonyum, periyodik tablonun 6. periyodunun 16. grubunda yer alan bir elementtir. Polonyumun atom numarası 84'dır. Polonyum, Po sembolü ile gösterilir ve metaldir.
Gümüşi renkte radyoaktif bir elementtir. Radyoaktif özelliğinden dolayı çok zehirlidir.
Alfa ışıması yapar. Paslanmaz çelik disklerin üzerine ince film şeklinde kaplanarak alfa parçacığı kaynağı olarak kullanılır. Bu diskler antistatik (elektrostatik boşalmayı azaltan ya da engelleyen) aygıtlarda ve bilimsel araştırmalarda kullanılır.
Berilyum ile karışımı ya da alaşımı nötron kaynağı olarak kullanılır.
85.Astatin (At)

Astatin, periyodik tablonun 6. periyodunun 17. grubunda yer alan bir elementtir. Astatinin atom numarası 85'dir. Astatin, At sembolü ile gösterilir ve ametaldir.
Tehlikeli derecede radyoaktif bir elementtir. Radyoaktif özelliğinden dolayı çok zehirlidir.
Çok küçük miktarlarda da olsa farklı yollardan elde edilebilir. Astatin-211 izotopu bizmut-200 izotopu nükleer reaktörlerde nötron bombardımanına tutularak elde edilebilir. Bilinen en uzun ömürlü izotopunun yarı ömrü 8 saattir.
Günümüzde sadece araştırma amaçlı kullanılıyor.
86.Radon (Rn)

Radon, periyodik tablonun 6. periyodunun 18. grubunda yer alan bir elementtir. Radonun atom numarası 86'dır. Radon, Rn sembolü ile gösterilir ve soy gazdır.
Renksiz ve kokusuz bir gazdır.
Kimyasal tepkimeye girmeye karşı isteksiz ancak radyoaktiftir.
Kayaçlarda bulunan radyum-226 izotopunun bozunması sonucu doğal olarak ortaya çıkar. Dünya atmosferinde ölçülebilecek düzeyde radon bulunur.
Bazı minerallerde örneğin granitte bulunan uranyumun bozunması sonucu radon gazı açığa çıkabilir.
Alfa ışıması yaparak polonyuma dönüşür. Bu bozunma sırasında yayılan radyasyon sebebiyle kanser tedavisinde kullanılır. Bazı hastanelerde radon gazı ufak tüplerin içine doldurulur ve bu tüpler kanserli dokulara nakledilerek tümörler yerinde tedavi edilir.
87.Fransiyum (Fr)

Fransiyum, periyodik tablonun 7. periyodunun 1. grubunda yer alan bir elementtir. Fransiyumun atom numarası 87'dir. Fransiyum, Fr sembolü ile gösterilir ve metaldir.
Son derece radyoaktif bir elementtir ve bu özelliğinden dolayı zehirlidir.
Yarı ömrü sadece 22 dakikadır. Herhangi bir kullanım alanı yoktur.
Radyumun nükleer reaktörlerde nötron bombardımanına tutulmasıyla elde edilir. Toryumun protonlarla bombardımana tutulmasıyla da üretilebilir.
88.Radyum (Ra)

Radyum, periyodik tablonun 7. periyodunun 2. grubunda yer alan bir elementtir. Radyumun atom numarası 88'dir. Radyum, Ra sembolü ile gösterilir ve metaldir.
Parlak, gümüşi renkte, yumuşak ve son derece radyoaktif bir elementtir. Radyoaktif özelliğinden dolayı zehirlidir ve kullanım alanı sınırlıdır.
Kemiklerde kalsiyum bulunur. Radyum periyodik tabloda kalsiyumla aynı grupta yer aldığı için kanserli kemik hücrelerini hedef almak için kullanılabilir. Radyum atomlarının yaptığı alfa ışıması kanserli hücrelerin yok edilmesini sağlar.
Tüm uranyum madenlerinde radyum da vardır. Ayrıca uranyum zenginleştirme işlemi sırasında yan ürün olarak da radyum elde edilebilir. Günümüzde nükleer reaktörlerde kullanılıp tükenmiş yakıt çubuklarından radyum elde ediliyor.
Demokratik Kongo Cumhuriyeti'ndeki ve Kanada'daki uranyum madenleri radyum bakımından en zengin madenlerdir. Radyumun yıllık üretimi 100 gramdan azdır. Alfa ışımasının yanı sıra gama ışınları da yaydığı için geçmişte kanser tedavisinde radyasyon kaynağı olarak kullanıldı.
89.Aktinyum (Ac)

Aktinyum, periyodik tablonun 7. periyodunun aktinitler grubunda yer alan 1. elementtir. Aktinyumun atom numarası 89'dur. Aktinyum, Ac sembolü ile gösterilir ve metaldir.
Gümüşi beyaz renkte, yumuşak ve radyoaktif bir metaldir. Radyoaktif özelliğinden dolayı zehirlidir. Yaydığı yoğun Çerenkov radyasyonu çevresindeki havayı uyardığı için karanlıkta bile mavi görünür.
Güçlü bir alfa parçacığı kaynağıdır.
Özellikle araştırma amaçlı kullanılır. Radyum-226 izotopunun nötron bombardımanına tutulmasıyla elde edilir. Uranyum madenlerinde de bulunur.
90. Toryum (Th)

Toryum, periyodik tablonun 7. periyodunun aktinitler grubunda yer alan 2. elementtir. Toryumun atom numarası 90'dır. Toryum, Th sembolü ile gösterilir ve metaldir.
Gümüşi renkte, düşük derecede radyoaktif bir metaldir. Radyoaktif özelliğinden dolayı zehirlidir.
Torit, uranotorit ve toriyanit madenlerinde bulunur. Toryumun ekonomik değeri en yüksek olan cevheri monazit madenidir.
Türkiye, dünyada ilk beş ülke arasına girecek miktarda toryum rezervine sahiptir.
Magnezyum ile alaşımlar oluşturarak malzemenin yüksek sıcaklıklardaki sertliğini ve sürtünme direncini artırır.
Nükleer enerji santrallerinde yakıt olarak kullanılabilecek potansiyele sahiptir. Doğadaki toryum miktarı kurşununkine hemen hemen eşit, uranyumunkininse üç katı kadardır. Toryumdan elde edilebilecek enerji miktarı uranyumdan ya da fosil yakıtlardan elde edilebilecek enerji miktarından muhtemelen daha fazladır.
Hindistan ve Çin, toryumun yakıt olarak kullanıldığı nükleer enerji santralleri geliştirmeye çalışıyor. Ancak bu teknolojinin henüz çok yeni olduğu söylenebilir.
91.Protaktinyum (Pa)

Gümüşi renkte, radyoaktif bir metaldir. Radyoaktif özelliğinden dolayı zehirlidir.
Uranyum madenlerinde az miktarlarda proaktinyum da bulunur. Ayrıca nükleer reaktörlerde kullanılıp tükenmiş yakıt çubuklarından da elde edilir.
Çoğunlukla araştırma amaçlı kullanılır.
92. Uranyum(U)

Uranyum, periyodik tablonun 7. periyodunun aktinitler grubunda yer alan 4. elementtir. Uranyumun atom numarası 92'dir. Uranyum, U sembolü ile gösterilir ve metaldir.
Gümüşi renkte, radyoaktif bir metaldir. Radyoaktif özelliğinden dolayı zehirlidir.
Uranit, brannerit ve karnotit madenlerinden doğal olarak çıkarılır. Dünya genelinde yılda 41 bin ton uranyum üretilir.
Nükleer enerji santrallerinde fisyon tepkimeleri sonucu enerji elde edilir ve yakıt olarak uranyum kullanılır. Nükleer enerji santrallerinde meydana gelen zincirleme çekirdek tepkimelerini kontrol altında tutmak için nötron soğurucu malzemeler kullanılır. Ortaya çıkan ısı enerjisi suyu buharlaştırır. Bu su buharıyla türbinler döndürülerek elektrik üretilir.
Uranyumdan daha ağır elementleri laboratuvar ortamında üretmek için kullanılan ana maddedir.
Doğadaki uranyumun yaklaşık %99'unu uranyum-238, yaklaşık %1'ini uranyum-235 izotopları oluşturur. Bu iki izotoptan sadece uranyum-235 nükleer enerji santrallerinde yakıt olarak kullanılabilir. Bu yüzden doğadan elde edilen uranyum madeninin nükleer reaktörlerde kullanılabilecek hâle gelmesi için önce uranyum-235 bakımından zenginleştirilmesi gerekir.
Nükleer bombalarda ve nükleer denizaltılara enerji sağlamak için de uranyum kullanılır.
93. Neptünyum (Np)

Neptünyum, periyodik tablonun 7. periyodunun aktinitler grubunda yer alan 5. elementtir. Neptünyumun atom numarası 93'tür. Neptünyum, Np sembolü ile gösterilir ve metaldir.
Radyoaktif bir metaldir. Radyoaktif özelliğinden dolayı zehirlidir.
Nükleer reaktörlerde yan ürün olarak elde edilir. Ayrıca tükenmiş uranyum yakıt çubuklarından da neptünyum elde edilir.
Uranyum madenlerinde eser miktarda neptünyum bulunur.
Neptünyum-237 izotopu nötron dedektörlerinde kullanılır.
Günümüzde çoğunlukla araştırma amaçlı kullanılıyor.
94.Plütonyum (Pu)

Plütonyum, periyodik tablonun 7. periyodunun aktinitler grubunda yer alan 6. elementtir. Plütonyumun atom numarası 94'tür. Plütonyum, Pu sembolü ile gösterilir ve metaldir.
Gümüşi renkte, radyoaktif bir metaldir. Radyoaktif özelliğinden dolayı zehirlidir.
Yapılan ilk atom bombalarının bazılarında plütonyum kullanılmıştı, günümüzde de nükleer silahların üretiminde kullanılıyor. Bir kilogram plütonyumun patlaması 10 bin tonluk bir kimyasal patlamaya eş değerdir.
Plütonyum nükleer enerji teknolojisinin gelişimi açısından önemli bir maddedir.
Çeşitli uzay görevlerinde -örneğin Mars'a gönderilen Curiosity ve Plüton'a doğru yol alan Yeni Ufuklar araçlarında- güç kaynağı olarak plütonyum kullanılıyor.
Nükleer reaktörlerde uranyumun bombardımana tutulmasıyla yarı ömrü 24.400 yıl olan plütonyum-239 izotopları ortaya çıkar. Bu süreç plütonyumun en önemli kaynağıdır.
95.Amerikyum (Am)

Amerikyum, periyodik tablonun 7. periyodunun aktinitler grubunda yer alan 7. elementtir. Amerikyumun atom numarası 95'tir. Amerikyum, Am sembolü ile gösterilir ve metaldir.
Parlak gümüşi renkte, radyoaktif bir metaldir. Radyoaktif özelliğinden dolayı zehirlidir.
Uranyum madenlerinde eser miktarda amerikyum bulunur. Elementi elde etmek için kullanılan ana yöntem, nükleer reaktörlerde plütonyumu nötron bombardımanına tutmaktır. Nükleer bombaların patlaması sonucunda da amerikyum ortaya çıkar.
Özellikle duman dedektörlerinde kullanılır.
Günümüzde uzay aracı bataryalarında plütonyum kullanılıyor. Ancak yeryüzündeki plütonyum miktarı çok kısıtlı olduğu için alternatifler üzerine araştırmalar yapılıyor. Gelecekte uzay aracı bataryalarında plütonyumun yerini almaya aday maddelerden biri de amerikyum.
96. Küriyum(Cm)

Küriyum, periyodik tablonun 7. periyodunun aktinitler grubunda yer alan 8. elementtir. Küriyumun atom numarası 96'dır. Küriyum, Cm sembolü ile gösterilir ve metaldir.
Gümüşi renkte, radyoaktif bir metaldir. Radyoaktif özelliğinden dolayı zehirlidir.
Havayla temas ettiğinde hızla matlaşır.
Uzay görevlerinde kullanılan elektrikli cihazlara güç sağlamak için kullanılır.
Nükleer reaktörlerde plütonyumun nötron bombardımanına tutulmasıyla üretilir. Uranyum madenlerinde de eser miktarda küriyum bulunur. Yılda sadece birkaç gram üretilir.
97.Berkelyum (Bk)

Berkelyum, periyodik tablonun 7. periyodunun aktinitler grubunda yer alan 9. elementtir. Berkelyumun atom numarası 97'dir. Berkelyum, Bk sembolü ile gösterilir ve metaldir.
Gümüşi renkte, radyoaktif bir metaldir. Radyoaktif özelliğinden dolayı zehirlidir.
Doğada bulunmaz, yapay bir elementtir.
Çok nadir bulunduğundan ticari veya teknolojik bir kullanım alanı yoktur.
Berkelyumu üretmek için kullanılan ana yöntem, plütonyum-239 izotoplarını nötron bombardımanına tutmaktır. Yıllık üretimi bir gramı geçmez.
98. Kaliforniyum (Cf)

Kaliforniyum, periyodik tablonun 7. periyodunun aktinitler grubunda yer alan 10. elementtir. Kaliforniyumun atom numarası 98'dir. Kaliforniyum, Cf sembolü ile gösterilir ve metaldir.
Radyoaktif bir metaldir. Radyoaktif özelliğinden dolayı zehirlidir.
Doğada bulunmaz, yapay bir elementtir.
Güçlü bir nötron yayıcısıdır. Altın ve gümüş cevherlerini tespit etmek için kullanılan portatif metal dedektörlerinde, petrol kuyularındaki su ve yağ katmanlarının belirlenmesinde, hava taşıtlarındaki metal yorgunluğunun tespit edilmesinde kullanılır.
Plütonyum-239 izotopunun nötron bombardımanına tutulmasıyla birkaç miligram kaliforniyum üretilebilir.
99.Aynştaynyum (Es)

Aynştaynyum, periyodik tablonun 7. periyodunun aktinitler grubunda yer alan 11. elementtir. Aynştaynyumun atom numarası 99'dur. Aynştaynyum, Es sembolü ile gösterilir ve metaldir.
Radyoaktif bir metaldir. Radyoaktif özelliğinden dolayı zehirlidir.
Doğada bulunmaz, yapay bir elementtir.
Yılda sadece birkaç miligram üretilir.
Nükleer reaktörlerde plütonyumun nötron bombardımanına tutulmasıyla birkaç miligram aynştaynyum üretilebilir.
Günümüzde sadece araştırma amaçlı üretiliyor.
100.Fermiyum (Fm)

Fermiyum, periyodik tablonun 7. periyodunun aktinitler grubunda yer alan 12. elementtir. Fermiyumun atom numarası 100'dür. Fermiyum, Fm sembolü ile gösterilir ve metaldir.
Radyoaktif bir metaldir. Radyoaktif özelliğinden dolayı zehirlidir.
Doğada bulunmaz, yapay bir elementtir.
Nükleer reaktörlerde plütonyumun nötron bombardımanına tutulmasıyla mikrogram ölçeğinde fermiyum üretilebilir.
Günümüzde sadece araştırma amaçlı üretiliyor.
101.Mendelevyum (Md)

Mendelevyum, periyodik tablonun 7. periyodunun aktinitler grubunda yer alan 13. elementtir. Mendelevyumun atom numarası 101'dir. Mendelevyum, Md sembolü ile gösterilir ve metaldir.
Radyoaktif bir metaldir.
Doğada bulunmaz, yapay bir elementtir.
Aynştaynyumun alfa parçacıklarıyla (helyum atomu çekirdekleriyle) bombardımana tutulması ile sadece birkaç atomu elde edilebildi.
Günümüzde sadece araştırma amaçlı üretiliyor.
102. Nobelyum (No)

Nobelyum, periyodik tablonun 7. periyodunun aktinitler grubunda yer alan 14. elementtir. Nobelyumun atom numarası 102'dir. Nobelyum, No sembolü ile gösterilir ve metaldir.
Radyoaktif bir metaldir. Radyoaktif özelliğinden dolayı zehirlidir. Yarı ömrü 58 dakikadır.
Doğada bulunmaz, yapay bir elementtir.
Siklotron adı verilen parçacık hızlandırıcılarda küriyum atomlarının karbon atomlarıyla bombardımana tutulması ile sadece birkaç atomu elde edilebildi.
Günümüzde sadece araştırma amaçlı üretiliyor.
103. Lavrensiyum (Lr)

Lavrensiyum, periyodik tablonun 7. periyodunun aktinitler grubunda yer alan 15. elementtir. Lavrensiyumun atom numarası 103'tür. Lavrensiyum, Lr sembolü ile gösterilir ve metaldir.
Radyoaktif bir metaldir.
Doğada bulunmaz, yapay bir elementtir.
Kaliforniyum atomlarının bor atomlarıyla bombardımana tutulmasıyla sadece birkaç atomu elde edilebildi.
Günümüzde sadece araştırma amaçlı üretiliyor.
104.Rutherfordyum (Rf)

Rutherfordyum, periyodik tablonun 7. periyodunun 4. grubunda yer alan bir elementtir. Rutherfordyumun atom numarası 104'tür. Rutherfordyum, Rf sembolü ile gösterilir ve metaldir.
Radyoaktif bir metaldir.
Doğada bulunmaz, yapay bir elementtir.
Kaliforniyum-249 izotoplarının karbon-12 izotoplarıyla bombardımana tutulmasıyla sadece birkaç atomu elde edilebildi.
Günümüzde sadece araştırma amaçlı üretiliyor.
105. Dubniyum (Db)

Dubniyum, periyodik tablonun 7. periyodunun 5. grubunda yer alan bir elementtir. Dubniyumun atom numarası 105'tir. Dubniyum, Db sembolü ile gösterilir ve metaldir.
Aşırı radyoaktif bir metaldir.
Doğada bulunmaz, yapay bir elementtir.
Kaliforniyum-249 izotoplarının azot-15 izotoplarıyla bombardımana tutulmasıyla sadece birkaç atomu elde edilebildi.
Günümüzde sadece araştırma amaçlı üretiliyor.
106. Siborgiyum (Sg)

Siborgiyum, periyodik tablonun 7. periyodunun 6. grubunda yer alan bir elementtir. Siborgiyumun atom numarası 106'dır. Siborgiyum, Sg sembolü ile gösterilir ve metaldir.
Radyoaktif bir elementtir.
Doğada bulunmaz, yapay bir elementtir.
Kaliforniyum-249 izotoplarının oksijen-18 izotoplarıyla bombardımana tutulmasıyla sadece birkaç atomu elde edilebildi.
Günümüzde sadece araştırma amaçlı üretiliyor.
107.Bohriyum (Bh)

Bohriyum, periyodik tablonun 7. periyodunun 7. grubunda yer alan bir elementtir. Bohriyumun atom numarası 107'dir. Bohriyum, Bh sembolü ile gösterilir ve metaldir.
Son derece radyoaktif bir metaldir.
Doğada bulunmaz, yapay bir elementtir.
Bizmut-209 izotoplarının krom-54 izotoplarıyla bombardımana tutulması ile sadece birkaç atomu elde edilebildi.
Günümüzde sadece araştırma amaçlı üretiliyor.
108.Hassiyum (Hs)

Hassiyum, periyodik tablonun 7. periyodunun 8. grubunda yer alan bir elementtir. Hassiyumun atom numarası 108'dir. Hassiyum, Hs sembolü ile gösterilir ve metaldir.
Son derece radyoaktif bir elementtir.
Doğada bulunmaz, yapay bir elementtir.
Kurşun atomlarının demir atomlarıyla bombardımana tutulması ile sadece birkaç atomu elde edilebildi.
Bilinen 15 izotopu vardır.
Günümüzde sadece araştırma amaçlı üretiliyor.
109.Metneryum (Mt)

Metneryum, periyodik tablonun 7. periyodunun 9. grubunda yer alan bir elementtir. Metneryumun atom numarası 109'dur. Metneryum, Mt sembolü ile gösterilir ve metaldir.
Son derece radyoaktif bir metaldir.
Doğada bulunmaz, yapay bir elementtir.
Bizmut atomlarının demir atomlarıyla bombardımana tutulmasıyla birkaç atomu elde edilebildi. Bilinen 7 tane izotopu vardır. En uzun ömürlü izotopunun yarı ömrü 8 saniyedir.
Günümüzde sadece araştırma amaçlı üretiliyor.
110. Darmstadtiyum (Ds)

Darmstadtiyum, periyodik tablonun 7. periyodunun 10. grubunda yer alan bir elementtir. Darmstadtiyumun atom numarası 110'dur. Darmstadtiyum, Ds sembolü ile gösterilir ve metaldir.
Son derece radyoaktif bir metaldir.
Doğada bulunmaz, yapay bir elementtir.
Nikel ve kurşun atomlarının füzyonuyla sadece birkaç atomu elde edilebildi.
Bilinen 7 tane izotopu vardır. En uzun ömürlü izotopunun yarı ömrü 22,8 saniyedir.
Günümüzde sadece araştırma amaçlı üretiliyor.
111.Röntgenyum (Rg)

Röntgenyum, periyodik tablonun 7. periyodunun 11. grubunda yer alan bir elementtir. Röntgenyumun atom numarası 111'dir. Röntgenyum, Rg sembolü ile gösterilir ve metaldir.
Son derece radyoaktif bir metaldir.
Doğada bulunmaz, yapay bir elementtir.
Nikel ve bizmut atomlarının füzyonuyla sadece birkaç atomu elde edilebildi.
Günümüzde sadece araştırma amaçlı üretiliyor.
112. Kopernikyum (Cn)

Kopernikyum, periyodik tablonun 7. periyodunun 12. grubunda yer alan bir elementtir. Kopernikyumun atom numarası 112'dir. Kopernikyum, Cn sembolü ile gösterilir ve metaldir.
Son derece radyoaktif bir metaldir. Kimyasal tepkimelere girmeye karşı isteksiz olduğu, bir metalden daha çok bir soy gaz gibi davrandığı düşünülüyor.
Doğada bulunmaz, yapay bir elementtir.
Kurşun ve çinko atomlarının füzyonuyla sadece birkaç atomu elde edilebildi.
Günümüzde sadece araştırma amaçlı üretiliyor.
113. Nihonyum (Nh)

Nihonyum, periyodik tablonun 7. periyodunun 13. grubunda yer alan bir elementtir. Nihonyumun atom numarası 113'tür. Nihonyum, Nh sembolü ile gösterilir.
Son derece radyoaktif bir metaldir.
Doğada bulunmaz, yapay bir elementtir.
Bilinen altı izotopu vardır.
Günümüzde sadece araştırma amaçlı üretiliyor.
114. Flerovyum (Fl)

Flerovyum, periyodik tablonun 7. periyodunun 14. grubunda yer alan bir elementtir. Flerovyumun atom numarası 114'tür. Flerovyum, Fl sembolü ile gösterilir.
Son derece radyoaktif bir metaldir.
Doğada bulunmaz, yapay bir elementtir.
Nükleer reaktörlerde üretilir. Bugüne kadar sadece birkaç atomu elde edilebildi.
Bilinen 4 izotopu vardır. En uzun ömürlü izotopu olan flerovyum-289'un yarı ömrü sadece 2,6 saniyedir.
Günümüzde sadece araştırma amaçlı üretiliyor.
115.Moskovyum (Mc)

Moskovyum, periyodik tablonun 7. periyodunun 15. grubunda yer alan bir elementtir. Moskovyumun atom numarası 115'tir. Moskovyum, Mc sembolü ile gösterilir.
Son derece radyoaktif bir metaldir.
Doğada bulunmaz, yapay bir elementtir.
Bilinen iki izotopu vardır.
Bugüne kadar sadece birkaç atomu elde edilebildi.
Günümüzde sadece araştırma amaçlı üretiliyor.
116.Livermoryum (Lv)

Livermoryum, periyodik tablonun 7. periyodunun 16. grubunda yer alan bir elementtir. Livermoryumun atom numarası 116'dır. Livermoryum, Lv sembolü ile gösterilir.
Son derece radyoaktif bir metaldir.
Doğada bulunmaz, yapay bir elementtir.
Küriyum atomlarının kalsiyum atomlarıyla bombardımana tutulmasıyla sadece birkaç atomu elde edilebildi.
Bilinen 4 izotopu vardır. En kararlı izotopunun yarı ömrü 53 milisaniyedir.
Günümüzde sadece araştırma amaçlı üretiliyor.
117. Tennessin (Ts)

Tennessin, periyodik tablonun 7. periyodunun 17. grubunda yer alan bir elementtir. Tennessinin atom numarası 117'dir. Tennessin, Ts sembolü ile gösterilir.
Son derece radyoaktif bir metaldir.
Doğada bulunmaz, yapay bir elementtir.
Bugüne kadar sadece birkaç atomu elde edilebildi.
Günümüzde sadece araştırma amaçlı üretiliyor.
118.Oganesson (Og)

Oganesson, periyodik tablonun 7. periyodunun 18. grubunda yer alan bir elementtir. Oganessonun atom numarası 118'dir. Oganesson, Og sembolü ile gösterilir.
Son derece radyoaktif bir metaldir.
Doğada bulunmaz, yapay bir elementtir.
Bugüne kadar sadece birkaç atomu elde edilebildi.
Günümüzde sadece araştırma amaçlı üretiliyor.
Devami...
